Нервные импульсы распространяются при перемещении ионов через мембрану нервной клетки и передаются из одной нервной клетки в другую с помощью нейромедиаторов.
В результате эволюции нервной системы человека и других животных возникли сложные информационные сети, процессы в которых основаны на химических реакциях. Важнейшим элементом нервной системы являются специализированные клетки нейроны. Нейроны состоят из компактного тела клетки, содержащего ядро и другие органеллы. От этого тела отходит несколько разветвленных отростков. Большинство таких отростков, называемых дендритами, служат точками контакта для приема сигналов от других нейронов. Один отросток, как правило самый длинный, называется аксоном и передает сигналы на другие нейроны. Конец аксона может многократно ветвиться, и каждая из этих более мелких ветвей способна соединиться со следующим нейроном.
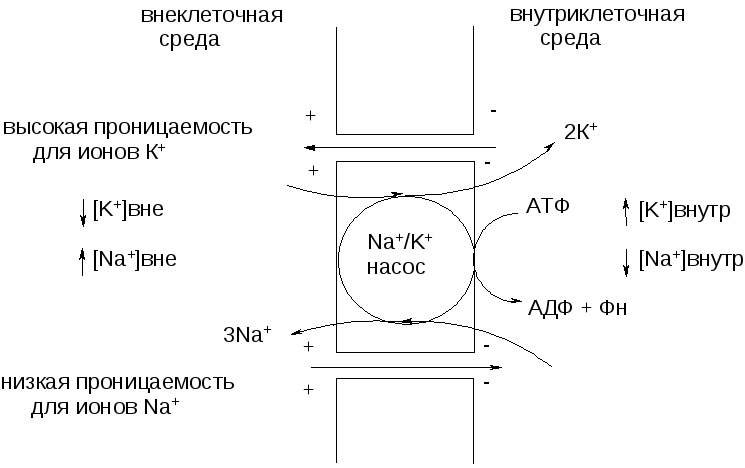
Во внешнем слое аксона находится сложная структура, образованная множеством молекул, выступающих в роли каналов, по которым могут поступать ионы — как внутрь, так и наружу клетки. Один конец этих молекул, отклоняясь, присоединяется к атому-мишени. После этого энергия других частей клетки используется на то, чтобы вытолкнуть этот атом за пределы клетки, тогда как процесс, действующий в обратном направлении, вводит внутрь клетки другую молекулу. Наибольшее значение имеет молекулярный насос, который выводит из клетки ионы натрия и вводит в нее ионы калия (натрий-калиевый насос).
Когда клетка находится в покое и не проводит нервных импульсов, натрий-калиевый насос перемещает ионы калия внутрь клетки и выводит ионы натрия наружу (представьте себе клетку, содержащую пресную воду и окруженную соленой водой). Из-за такого дисбаланса разность потенциалов на мембране аксона достигает 70 милливольт (приблизительно 5% от напряжения обычной батарейки АА).
Однако при изменении состояния клетки и стимуляции аксона электрическим импульсом равновесие на мембране нарушается, и натрий-калиевый насос на короткое время начинает работать в обратном направлении. Положительно заряженные ионы натрия проникают внутрь аксона, а ионы калия откачиваются наружу. На мгновение внутренняя среда аксона приобретает положительный заряд. При этом каналы натрий-калиевого насоса деформируются, блокируя дальнейший приток натрия, а ионы калия продолжают выходить наружу, и исходная разность потенциалов восстанавливается. Тем временем ионы натрия распространяются внутри аксона, изменяя мембрану в нижней части аксона. При этом состояние расположенных ниже насосов меняется, способствуя дальнейшему распространению импульса. Резкое изменение напряжения, вызванное стремительными перемещения ионов натрия и калия, называют потенциалом действия. При прохождении потенциала действия через определенную точку аксона, насосы включаются и восстанавливают состояние покоя.
Потенциал действия распространяется довольно медленно — не более доли дюйма за секунду. Для того чтобы увеличить скорость передачи импульса (поскольку, в конце концов, не годится, чтобы сигнал, посланный мозгом, достигал руки лишь через минуту), аксоны окружены оболочкой из миелина, препятствующей притоку и оттоку калия и натрия. Миелиновая оболочка не непрерывна — через определенные интервалы в ней есть разрывы, и нервный импульс перескакивает из одного «окна» в другое, за счет этого скорость передачи импульса возрастает.
Когда импульс достигает конца основной части тела аксона, его необходимо передать либо следующему нижележащему нейрону, либо, если речь идет о нейронах головного мозга, по многочисленным ответвлениям многим другим нейронам. Для такой передачи используется абсолютно иной процесс, нежели для передачи импульса вдоль аксона. Каждый нейрон отделен от своего соседа небольшой щелью, называемой синапсом. Потенциал действия не может перескочить через эту щель, поэтому нужно найти какой-то другой способ для передачи импульса следующему нейрону. В конце каждого отростка имеются крошечные мешочки, называющие (пресинаптическими) пузырьками, в каждом из которых находятся особые соединения — нейромедиаторы. При поступлении потенциала действия из этих пузырьков высвобождаются молекулы нейромедиаторов, пересекающие синапс и присоединяющиеся к специфичным молекулярным рецепторам на мембране нижележащих нейронов. При присоединении нейромедиатора равновесие на мембране нейрона нарушается. Сейчас мы рассмотрим, возникает ли при таком нарушении равновесия новый потенциал действия (нейрофизиологи продолжают искать ответ на этот важный вопрос до сих пор).
После того как нейромедиаторы передадут нервный импульс от одного нейрона на следующий, они могут просто диффундировать, или подвергнуться химическому расщеплению, или вернуться обратно в свои пузырьки (этот процесс нескладно называется обратным захватом). В конце XX века было сделано поразительное научное открытие — оказывается, лекарства, влияющие на выброс и обратный захват нейромедиаторов, могут коренным образом изменять психическое состояние человека. Прозак (Prozac*) и сходные с ним антидепрессанты блокируют обратный захват нейромедиатора серотонина. Складывается впечатление, что болезнь Паркинсона взаимосвязана с дефицитом нейромедиатора допамина в головном мозге. Исследователи, изучающие пограничные состояния в психиатрии, пытаются понять, как эти соединения влияют на человеческий рассудок.
По-прежнему нет ответа на фундаментальный вопрос о том, что же заставляет нейрон инициировать потенциал действия — выражаясь профессиональным языком нейрофизиологов, неясен механизм «запуска» нейрона. В этом отношении особенно интересны нейроны головного мозга, которые могут принимать нейромедиаторы, посланные тысячей соседей. Об обработке и интеграции этих импульсов почти ничего не известно, хотя над этой проблемой работают многие исследовательские группы. Нам известно лишь, что в нейроне осуществляется процесс интеграции поступающих импульсов и выносится решение, следует или нет инициировать потенциал действия и передавать импульс дальше. Этот фундаментальный процесс управляет функционированием всего головного мозга. Неудивительно, что эта величайшая загадка природы остается, по крайней мере сегодня, загадкой и для науки!
См. также:
Механизм возникновения и проведения нервного импульса
Возникновение
нервного импульса связано с состоянием
мембраны нейрона. Биологические мембраны,
будучи липидно-белковым комплексом,
непроницаемы для заряженных ионов.
Перемещение ионов через мембрану
осуществляется с помощью специальных
транспортных систем: натриевого насоса,
работающего с затратой энергии (Na+,
К+-АТФ-аза)
и ионпроводящих каналов – натриевых и
калиевых.
В состоянии
физиологического покоя по разные стороны
мембраны имеет место разность концентраций
ионов, главным образом Na+
и К+.
Концентрация ионов К+
выше в
клетке,
ионов Na+
– в межклеточной жидкости. Это влияет
и на распределение других ионов. Разность
концентраций ионов поддерживается с
помощью натриевого насоса, перекачивающего
ионы против градиента концентрации (в
противном случае диффузия ионов по
градиенту концентрации привела бы к
выравниванию концентраций ионов по обе
стороны мембраны и гибели клетки) Таким
образом, внутри аксона образуется
избыток (–) зарядов, снаружи – (+) зарядов,
то есть возникает разность электрических
потенциалов – потенциал покоя (ПП). Его
значение составляет – 60-70 мВ. ПП одинаков
по всей длине нервного волокна (рис. 4).
Раздражение
нервного волокна приводит сначала к
открытию Na+—
и К+—
каналов. Раньше открываются Na+-каналы,
и в клетку устремляется поток ионов
натрия. Это изменяет трансмембранный
потенциал: сначала он становится равным
0 (деполяризация мембраны), затем
происходит перезарядка мембраны,
внутренняя сторона мембраны приобретает
(+) заряд, наружная (-). Разность потенциалов
при этом достигает 40 мВ. Эта величина и
есть потенциал действия (ПД) (рис. 5).
Рис. 4. Природа поляризации клеточной
мембраны
Натриевые каналы
закрываются, открываются калиевые,
начинается выход калия из клетки,
потенциал изменяется от – 40 мВ до – 70
мВ, то есть идет реполяризация мембраны.
После закрытия ионных каналов ионный
насос восстанавливает исходное
распределение ионов по сторонам мембраны.
Рис. 5. Потенциал действия
ПД развивается в
том случае, если под действием раздражителя
происходит изменение ПП до -50 мВ (пороговое
значение). Если действие раздражителя
не достигает этого значения, ПД не
генерируется (принцип «все или ничего»).
Движение пд по аксону
Потенциал действия,
возникая в одном участке аксона,
вследствие диффузии ионов вдоль нервного
волокна изменяет ПП в соседнем участке
и вызывает развитие ПД. Благодаря этому
ПД, возникнув в одном месте, проходит
весь аксон и достигает следующей клетки.
В таком качестве ПД называется нервным
импульсом.
В миелиновом
волокне Na+—
и К+—
каналы располагаются в перехватах
Ранвье, где мембрана аксона контактирует
с межклеточной жидкостью. Поэтому
распространение нервного импульса идет
скачками; скорость распространения
импульса в 5-6 раз выше, чем в безмиелиновом
волокне, где ПД распространяется плавно.
Вся деятельность
нервной системы строится на основе
рефлексов, материальной основой которых
являются рефлекторные дуги. Рефлекторной
дугой
называется путь, состоящий из цепей
нейронов, по которому нервный импульс
проходит от чувствительных нервных
клеток до рабочего органа. Рефлекторные
дуги могут быть простыми или сложными.
Простая рефлекторная дуга состоит из
двух нейронов – чувствительного и
двигательного (эффекторного), между
которыми один синапс.
Примерами простых
рефлекторных дуг являются дуги сухожильных
рефлексов (коленного, ахиллова,
подошвенного, сгибательного и
разгибательного локтевого, брюшного),
которые замыкаются на уровне спинного
мозга.
Рис. 6. Рефлекторная дуга кожного рефлекса
Рефлекторные дуги
большинства рефлексов включат помимо
чувствительного и эффекторного еще
несколько вставочных нейронов. Посредством
вставочных нейронов осуществляется
контроль адекватности ответа рабочего
органа полученному раздражению (рис.
6).
Вегетативные
рефлекторные дуги являются кольцевыми,
от рабочего органа есть обратная связь
в ЦНС для регуляции рефлекторной реакции.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
В теле человека бессчетное количество клеток, каждая из которых имеет собственную функцию. Среди них самые загадочные – нейроны, отвечающие за любое совершаемое нами действие. Попробуем разобраться как работают нейроны и в чем их предназначение.
Что такое нейрон (нейронные связи)
В переводе с греческого нейрон, или как его еще называют неврон, означает «волокно», «нерв». Нейрон – это специфическая структура в нашем организме, которая отвечает за передачу внутри него любой информации, в быту называемая нервной клеткой.
Нейроны работают при помощи электрических сигналов и способствуют обработке мозгом поступающей информации для дальнейшей координации производимых телом действий.
Эти клетки являются составляющей частью нервной системы человека, предназначение которой состоит в том, чтобы собрать все сигналы, поступающие из вне или от собственного организма и принять решение о необходимости того или иного действия. Именно нейроны помогают справиться с такой задачей.
Каждый из нейронов имеет связь с огромным количеством таких же клеток, создаётся своеобразная «паутина», которая называется нейронной сетью. Посредством данной связи в организме передаются электрические и химические импульсы, приводящие всю нервную систему в состояние покоя либо, наоборот, возбуждения.
К примеру, человек столкнулся с неким значимым событием. Возникает электрохимический толчок (импульс) нейронов, приводящий к возбуждению неровной системы. У человека начинает чаще биться сердце, потеют руки или возникают другие физиологические реакции.
Мы рождаемся с заданным количеством нейронов, но связи между ними еще не сформированы. Нейронная сеть строится постепенно в результате поступающих из вне импульсов. Новые толчки формируют новые нейронные пути, именно по ним в течение жизни побежит аналогичная информация. Мозг воспринимает индивидуальный опыт каждого человека и реагирует на него. К примеру, ребенок, схватился за горячий утюг и отдернул руку. Так у него появилась новая нейронная связь.
Стабильная нейронная сеть выстраивается у ребенка уже к двум годам. Удивительно, но уже с этого возраста те клетки, которые не используются, начинают ослабевать. Но это никак не мешает развитию интеллекта. Наоборот, ребенок познает мир через уже устоявшиеся нейронные связи, а не анализирует бесцельно все вокруг.
Даже у такого малыша есть практический опыт, позволяющий отсекать ненужные действия и стремиться к полезным. Поэтому, например, так сложно отучить ребенка от груди — у него сформировалась крепкая нейронная связь между приложением к материнскому молоку и удовольствию, безопасности, спокойствию.
Познание нового опыта на протяжении всей жизни приводит к отмиранию ненужных нейронных связей и формированию новых и полезных. Этот процесс оптимизирует головной мозг наиболее эффективным для нас образом. Например, люди, проживающие в жарких странах, учатся жить в определенном климате, а северянам нужен совсем другой опыт для выживания.
Сколько нейронов в мозге
Нервные клетки в составе головного мозга занимают порядка 10 процентов, остальные 90 процентов это астроциты и глиальные клетки, но их задача заключается лишь в обслуживании нейронов.
Подсчитать «вручную» численность клеток в головном мозге также сложно, как узнать количество звезд на небе.
Тем не менее ученые придумали сразу несколько способов для определения количества нейронов у человека:
- Рассчитывается число нервных клеток на небольшой части мозга, а затем, количество умножается пропорционально полному объему. Исследователи исходят из постулата о том, что нейроны равномерно распределены в нашем мозге.
- Происходит растворение всех мозговых клеток. В результате получается жидкость, в составе которой можно увидеть клеточные ядра. Их можно посчитать. При этом служебные клетки, о которых мы сказали выше, не учитываются.
В результате описанных экспериментов установлено, что число нейронов в головном мозге человека — 85 миллиардов единиц. Ранее, на протяжении многих веков считалось, что нервных клеток больше, порядка 100 миллиардов.
Строение нейрона
На рисунке приведено строение нейрона. Он состоит из основного тела и ядра. От клеточного тела идет ответвление многочисленных волокон, которые именуются дендритами.
Мощные и длинные дендриты называются аксонами, которые в действительности намного длиннее, чем на картинке. Их протяженность варьируется от нескольких миллиметров до более метра.
Аксоны играют ведущую роль в передаче информации между нейронами и обеспечивают работу всей нервной системы.
Место соединения дендрита (аксона) с другим нейроном называется синапсом. Дендриты при наличии раздражителей могут разрастись настолько сильно, что станут улавливать импульсы от других клеток, что приводит к образованию новых синаптических связей.
Синаптические связи играют существенную роль в формировании личности человека. Так, личность с устоявшимся позитивным опытом будет смотреть на жизнь с любовью и надеждой, человек, у которого нейронные связи с негативным зарядом, станет со временем пессимистом.
Виды нейронов и нейронных связей
Нейроны можно обнаружить в различных органах человека, а не исключительно в головном мозге. Большое их количество расположено в рецепторах (глаза, уши, язык, пальцы рук – органы чувств). Совокупность нервных клеток, которые пронизывают наш организм составляет основу периферической нервной системы. Выделим основные виды нейронов.
| Вид нейронной клетки | За что отвечает |
|---|---|
| Аффекторные | Являются переносчиками информации от органов чувств в головной мозг. У этого вида нейронов самые длинные аксоны. Импульс из вне поступает по аксонам строго в определенный участок головного мозга, звук — в слуховой «отсек», запах – в «обонятельный» и т.д. |
| Промежуточные | Промежуточные нервные клетки обрабатывают сведения, поступившие от аффекторных нейронов и передают ее периферическим органам и мышцам. |
| Эффекторные | На заключительном этапе в дело вступают эфференты, которые доводят команду промежуточных нейронов до мышц и других органов тела. |
Слаженная работа нейронов трех типов выглядит так: человек «слышит» запах шашлыка, нейрон передает информацию в соответствующий раздел мозга, мозг передает сигнал желудку, который выделяет желудочный сок, человек принимает решение «хочу есть» и бежит покупать шашлык. Упрощенно так это действует.
Самыми загадочными являются промежуточные нейроны. С одной стороны, их работа обуславливает наличие рефлекса: дотронулся до электричества – отдернул руку, полетела пыль –зажмурился. Однако, пока не объяснимо как обмен между волокнами рождает идеи, образы, мысли?
Единственное, что установили ученые, это тот факт, что любой вид мыслительной деятельности (чтение книг, рисование, решение математических задач) сопровождается особой активностью (вспышкой) нервных клеток определенного участка головного мозга.
Есть особая разновидность нейронов, которые именуются зеркальными. Их особенность заключается в том, что они не только приходят в возбуждение от внешних сигналов, но и начинают «шевелиться», наблюдая за действиями своих собратьев – других нейронов.
Функции нейронов
Без нейронов невозможна работа организма человека. Мы увидели, что эти наноклетки отвечают буквально за каждое наше движение, любой поступок. Выполняемые ими функции до настоящего времени в полной мере не изучены и не определены.
Существует несколько классификаций функций нейронов. Мы остановимся на общепринятой в научном мире.
Функция распространения информации
Данная функция:
- является основной;
- изучена лучше остальных.
Суть ее в том, что нейронами обрабатываются и переносятся в головной мозг все импульсы, которые поступают из окружающего мира или собственного тела. Далее происходит их обработка, подобно тому, как работает поисковик в браузере.
По результатам сканирования сведений из вне, головной мозг в форме обратной связи передает обработанную информацию к органам чувств или мышцам.
Мы не подозреваем, что в нашем теле происходит ежесекундная доставка и переработка информации, не только в голове и на уровне периферической нервной системы.
До настоящего времени создать искусственный интеллект, который бы приблизился к работе нейронных сетей человека, не удалось. У каждого из 85 миллиардов нейронов имеется, как минимум, 10 тысяч обусловленных опытом связей, и все они работают на передачу и обработку информации.
Функция аккумуляции знаний (сохранения опыта)
Человек обладает памятью, возможностью понимать суть вещей, явлений и действий, которые он единожды или многократно повторял. За формирование памяти отвечают именно нейронные клетки, точнее нейротрансмиттеры, связующие звенья между соседними нейронами.
Таким образом, за память отвечает не какая-то отдельная часть мозга, а маленькие белковые мостики между клетками. Человек может потерять память, когда произошло крушение этих нервных связей.
Функция интеграции
Данная функция позволяет взаимодействовать между собой отдельным долям головного мозга. Как мы уже сказали, сигналы от разных органов чувств поступают в разные отделы мозга.
Нейроны посредством «вспышек» активности передают и принимают импульсы в разных частях мозга. Так происходит процесс появления мыслей, эмоций и чувств. Чем больше таких разноплановых связей, тем эффективнее человек мыслит. Если человек способен к размышлениям и аналитике в определенном направлении, то он будет хорошо соображать и в другом вопросе.
Функция производства белков
Нейроны – настолько полезные клетки, что не ограничиваются только передаточными функциями. Нервные клетки вырабатывают необходимые для жизни человека белки. Опять же ключевую роль в производстве белков имеют нейротрансмиттеры, которые отвечают за память.
Всего в невронах индуцируется порядка 80 белков, вот основные из них, влияющие на самочувствие человека:
- Серотонин – вещество, вызывающее радость и удовольствие.
- Допамин – ведущий источник бодрости и счастья для человека. Активизирует физическую активность, помогает проснуться, переизбыток может привести к состоянию эйфории.
- Норадреналин – это «плохой» гормон, вызывающий приступы ярости и гнева. Наряду с кортизолом его называют гормоном стресса.
- Глутамат – вещество, отвечающие за хранение памяти.
Прекращение выработки белков или их выпуск в недостаточном количестве способны привести к тяжелым заболеваниям.
Восстанавливаются ли нервные клетки
При нормальном состоянии организма нейроны могут жить и функционировать очень долго. К сожалению, случается так, что они начинают массово погибать. Причин разрушения нервных волокон может быть много, но до конца механизм их деструкции не изучен.
Установлено, что нервные клетки погибают из-за гипоксии (кислородное голодание). Нейронные сети рушатся при отдельных травмах головного мозга, человек теряет память или утрачивает способность к хранению информации. В этом случае сами нейроны сохранены, но теряется их передаточная функция.
Отсутствие допамина ведет к развитию болезни Паркинсона, а его переизбыток является причиной шизофрении. Почему прекращается выработка белка не известно, спусковой механизм не выявлен.
Гибель нервных клеток происходит при алкоголизации личности. Алкоголик со временем может совершенно деградировать и утратить вкус к жизни.
Формирование нервных клеток происходит при рождении. Долгое время ученые полагали, что со временем нейроны отмирают. Поэтому с возрастом человек утрачивает способность накапливать информацию, хуже соображает. Нарушение функции по выработке допамина и серотонина связывается с наличием практически у всех пожилых людей депрессивных состояний.
Гибель нейронов, действительно неизбежна, в год исчезает примерно 1 процент от их количества. Но есть и хорошие новости. Последние исследования показали, что в коре головного мозга есть особенный участок, именуемый гипокаммом. Именно в нем генерируются новые чистые нейроны. Подсчитано примерное количество генерируемых ежедневно нервных клеток – 1400.
В науке обозначилось новое понятие «нейропластичность», обозначающее возможность мозга регенерироваться и перестраиваться. Но есть одна тонкость: новые нейроны еще не имеют никакого опыта и наработанных связей. Поэтому с возрастом или после заболевания мозг нужно тренировать, как и все иные мышцы тела: получать новые знания, анализировать происходящие события и явления.
Подобно тому, как мы усиливаем бицепс при помощи гантели, активизировать процесс включения новых нервных клеток можно следующими способами:
- изучение новых сфер знаний, которые ранее были не нужны или не интересны. К примеру, математику можно начать изучать живопись, а юристу – основы физики.
- через постановку сложных задач и поиск их решения;
- составлением планов деятельности, которые включают в себя множество исходных данных.
Механизм возрождения прост. У нас имеются совершенно не задействованные новые клетки, которые нужно заставить работать, а сделать это можно лишь путем постановки новых задач и изучения неизвестных предметных сфер.
Вся информация взята из открытых источников.
Если вы считаете, что ваши авторские права нарушены, пожалуйста,
напишите в чате на этом сайте, приложив скан документа подтверждающего ваше право.
Мы убедимся в этом и сразу снимем публикацию.
В нейроне генерируется и по аксону посылается потенциал действия, который затем передается на синапс посредством выделения нейротрансмиттеров, вызывающих ответную реакцию в другом нейроне или эффекторной клетке (например, мышечные клетки, большинство экзокринных и эндокринных клеток). Нейротрансмиттеры позволяют нейронам общаться друг с другом. Высвобождающиеся нейротрансмиттеры связываются с рецепторами другого нейрона. Нейроны, которые выделяют нейротрансмиттеры, называются пресинаптическими нейронами. Нейроны, которые получают нейротрансмиттерные сигналы, называются постсинаптическими нейронами. В зависимости от типа нейротрансмиттера и рецептора, сигнал может или активировать, или тормозить воспринимающую клетку. Другие факторы, в том числе лекарства и расстройства, влияют на связь между нейронами, модулируя выработку и действие нейротрансмиттеров, в том числе
-
Их высвобождение, обратный захват и распад
-
Количество и функция постсинаптических нейромедиаторных рецепторов
Иногда сигналы между нейронами проходят в обратном направлении (так называемая ретроградная нейротрансмиссия). В таких случаях дендриты (приемные ветви нейрона) постсинаптических нейронов высвобождают нейротрансмиттеры, которые влияют на рецепторы пресинаптических нейронов. Ретроградная передача может препятствовать высвобождению дополнительных нейротрансмиттеров пресинаптическими нейронами и помочь контролировать уровень активности и связи между нейронами.
Межклеточные взаимодействия в центральной нервной системе (ЦНС) очень сложны. Импульс от одного нейрона к другому может проходить от
-
аксона к телу клетки
-
аксона к дендриту
-
тела клетки к телу клетки
-
дендрита к дендриту
Нейрон воспринимает одновременно огромное количество импульсов – как возбуждающих, так и тормозящих – от других нейронов, и эти сигналы объединяет в различные паттерны разрядов.
Проведение потенциала действия по аксону имеет электрическую природу и вызвано переходом ионов натрия и калия через мембрану аксона. Отдельный нейрон генерирует однотипные сигналы после каждого стимула, проводя их с фиксированной скоростью по аксону. Скорость проведения зависит от диаметра аксона и степени его миелинизации и составляет от 1–4 м/секунду для малых немиелинизированных волокон до 75 м/секунду в крупных миелинизированных. Распространение импульса происходит с намного большей скоростью в миелинизированных волокнах, поскольку по ходу миелиновой оболочки с равной частотой располагаются промежутки (перехваты Ранвье), где обнажается мембрана аксона. Электрический импульс «перепрыгивает» с одного перехвата к другому, пропуская миелинизированный участок аксона. Вследствие этого при заболеваниях, нарушающих миелиновую оболочку (например, рассеянный склероз Рассеянный склероз (РС) Рассеянный склероз (РС) характеризуется появлением в головном и спинном мозге диссеминированных очагов демиелинизации. Характерные симптомы включают зрительные и глазодвигательные нарушения… Прочитайте дополнительные сведения 
Передача импульса имеет химическую природу и вызывается высвобождением определенных нейромедиаторов из нервного окончания. Медиаторы диффундируют через синаптическую щель и на короткое время связываются со специфическими рецепторами на эффекторной клетке. В зависимости от рецептора результатом взаимодействия может быть как возбуждение, так и торможение. Обычно нейроны не касаются друг друга; вместо этого они общаются посредством трансмиссии нейромедиаторов через синапсы. При некоторых условиях нейроны рядом друг с другом могут общаться с помощью электрических импульсов через щелевое соединение.
В теле нейрона вырабатываются ферменты, синтезирующие большинство медиаторов, которые затем хранятся в везикулах нервного окончания (см. рисунок Нейротрансмиссия Нейротрансмиссия 
Один из подвидов синапсов, электрический синапс, не включает высвобождение нейромедиаторов; цитоплазмы пре- и постсинаптического нейронов непосредственно связывают ионные каналы. Эта разновидность соединения является наиболее быстрой.
Возбуждающие и тормозящие импульсы
Реакция, вызванная высвобождением нейротрансмиттера, может либо возбуждать или активировать постсинаптический нейрон, либо ингибировать или блокировать его активность. Постсинаптические нейроны получают множественные нейромедиаторные и электрические сигналы от многих нейронов. Принимающий нейрон в конечном итоге складывает входящие данные вместе, и, если поступает больше возбуждающих сигналов, нейрон «выстреливает» и посылает сигналы другим нейронам. Если сумма сигналов является ингибирующей, нейрон не «выстреливает» и не оказывает влияния на активность других нейронов. Это сочетание реакций называется суммированием. Нейротрансмиттеры, таким образом, способствуют быстрой связи между нейронами, изменяя возбуждение потенциала действия.
Другие формы суммирования включают
-
Пространственная суммация: когда нейрон получает несколько импульсов в разных местах, он затем их суммирует
-
Временное суммирование: когда импульсы получены в течение короткого периода времени, а затем суммируются
Чтобы нейрон генерировал сигнал и выстрелил, он должен достичь порогового потенциала. Пороговый потенциал создается за счет чистого увеличения притока натрия в клетку во время обмена ионов натрия и калия. Когда в клетку поступает достаточное количество натрия, достигается пороговая величина; при достижении пороговой величины срабатывает потенциал действия; он движется вдоль мембраны нейрона. Порог должен быть достигнут для создания потенциала действия.
Нейротрансмиссия
Потенциалы действия открывают аксональные кальциевые каналы (не показано). Ca++ активирует высвобождение нейромедиаторов (НМ) из везикул. НМ заполняют синаптическую щель. Некоторые из них связываются с постсинаптическими рецепторами, вызывая ответную реакцию. Остальные подвергаются обратному захвату в аксон, где накапливаются, или диффундируют в окружающие ткани.
Количество нейромедиаторов в нервном окончании не зависит от активности нейрона и сохраняется относительно постоянным благодаря непрерывной модификации процессов захвата предшественников нейромедиатора и активности ферментов, синтезирующих и разрушающих нейромедиатор. Стимуляция пресинаптических рецепторов может уменьшить пресинаптический синтез нейромедиатора, а их блокада может его увеличить.
Взаимодействие нейромедиатора с рецептором для окончания продолжающегося действия трансмиттера и/или с целью обеспечения быстрой повторной активации рецепторов должно быть достаточно коротким. После связывания нейротрансмиттеров с рецепторами возможен один из следующих вариантов:
-
С целью повторного использования или уничтожения нейромедиаторы быстро захватываются обратно в пресинаптическое нервное окончание активным АТФ-зависимым транспортом (обратный захват).
-
Они могут быть устранены ферментами вблизи рецепторов.
-
Нейротрансмиттеры диффундируют в окружающие ткани.
При обратном захвате нейромедиаторов нервными окончаниями происходит их накопление в гранулах или везикулах на концевых участках аксонов – для повторного высвобождения.
Нарушение этих процессов может привести к клиническому заболеванию. Например, считается, что потеря памяти при болезни Альцгеймера связана с недостаточностью нейротрансмиттера ацетилхолина в синапсах, что способствует закладыванию новых воспоминаний. Некоторые лекарства (например, донепезил, галантамин, ривастигмин) блокируют фермент ацетилхолинэстеразу (которая расщепляет ацетилхолин) и, таким образом, увеличивают количество ацетилхолина в синапсе. В результате может улучшиться функция памяти.
Некоторые типы отдельных нейронов могут выделять два или более различных нейротрансмиттеров (называемых котрансмиссией) — например, ацетилхолин и глутамат. Множество нейротрансмиттеров могут воздействовать на один постсинаптический нейрон или влиять на множество постсинаптических нейронов. Котрансмиссия позволяет осуществлять сложную связь между нейронами для контроля различных событий в ЦНС и периферической нервной системе (ПНС).
Нейротрансмиттеры могут также способствовать более длительным изменениям, которые включают дополнительные пути, например, изменения активности генов и белков.
Рецепторы к нейромедиаторам представляют собой белковые комплексы, расположенные на клеточной мембране. Именно от их природы зависит, будет ли влияние отдельно взятого нейромедиатора возбуждающим или тормозным. В случае если рецепторы постоянно стимулируются медиаторами или определенными препаратами, их чувствительность снижается; те рецепторы, которые не стимулируются нейромедиаторами или при их хронической медикаментозной блокаде, они становятся сверхчувствительными (открытые рецепторы). Указанные процессы сильно влияют на развитие толерантности и физической зависимости. Особую значимость эти принципы приобретают в случаях трансплантации органов или тканей, при которой денервация лишает рецепторы возможности связываться с нейромедиаторами; в результате трансплантированные органы могут стать чрезмерно чувствительными к нервной стимуляции. Синдром отмены частично можно объяснить феноменом «рикошета» из-за измененной аффинности или плотности рецепторов.
Большинство нейромедиаторов взаимодействуют с постсинаптическими рецепторами, однако некоторые рецепторы расположены на пресинаптических нейронах, обеспечивая точное регулирование высвобождения нейротрансмиттера.
Одна из групп рецепторов, называемая ионотропными рецепторами (например, рецепторы N-метил-D-глутамата, каината, ацетилхолина, глицина и гамма-аминомасляной кислоты [ГАМК]), состоит из ионных каналов, которые открываются при связывании с нейромедиатором, приводя к возникновению быстрого ответа. В другой группе метаботропные рецепторы (например, рецепторы к серотонину, альфа- и бета-адренорецепторы, допаминергические рецепторы), нейромедиаторы взаимодействуют с G-белком и активируют молекулу-посредник (вторичный «мессенджер», например, цАМФ), являющийся катализатором целого каскада реакций, реализующихся посредством фосфорилизации белков и/или мобилизации ионов кальция; изменения, происходящие в клетке под воздействием вторичных молекул-посредников, медленнее, чем в 1-ой группе рецепторов, однако они позволяют обеспечить более точную регуляцию быстрого ионотропного ответа. Большинство медиаторов активируют специфичные им рецепторы, меньшая часть – вторичные мессенджеры.
По крайней мере 100 молекул могут выступать в роли нейромедиаторов; из них 18 имеют первостепенное значение. Некоторые встречаются в различных формах. Нейротрансмиттеры могут быть сгруппированы в разные классы, такие как
-
Небольшие молекулы (например, глутамат, гамма-аминомасляная кислота, глицин, аденозин, ацетилхолин, серотонин, гистамин, норадреналин)
-
Нейропептиды (например, эндорфины)
-
Газообразные молекулы (например, оксид азота, оксид углерода)
-
Эндоканнабиноиды
Эти аминокислоты (глутамат и аспартат) являются основными возбуждающими нейромедиаторами в ЦНС. Их обнаруживают в коре головного мозга, мозжечке и спинном мозге. В ответ на воздействие глутамата в нейронах повышается синтез оксида азота (NO). Избыточная концентрация глутамата может оказывать токсическое действие, повышая уровень внутриклеточного кальция, свободных радикалов и активность протеиназ. Эти нейромедиаторы участвуют в развитии толерантности к опиоидам и опосредуют развитие гипералгезии.
Глутаматные рецепторы (стимулируемые глутаматом и менее сильно аспартатом) классифицируются как NMDA (N-метил-d-аспартат) и не-NMDA рецепторы. Фенциклидин (ФЦД, также известный под названием «ангельская пыль» [в РФ не зарегистрирован]) и мемантин (применяемый в лечении болезни Альцгеймера) связываются с рецепторами NMDA.
Гамма-аминобутировая кислота (ГАМК) – основной тормозной нейромедиатор в мозге. Это аминокислота, синтезируемая из глутаминовой кислоты посредством декарбоксилирования глутаматдекарбоксилазой. После взаимодействия с рецепторами ГАМК активно захватывается обратно в нервные окончания и метаболизируется. Глицин, который по действию напоминает ГАМК, встречается преимущественно во вставочных нейронах (клетки Реншоу) спинного мозга и в нейронных цепях, расслабляющих мышцы-антагонисты.
Разделяют GABA-A (активирующие хлорные каналы) и GABA-B (активирующие образование цАМФ) рецепторы. GABA-A-рецепторы являются точкой приложения для нескольких нейроактивных препаратов, включая бензодиазепины, барбитураты, пикротоксин и мусцимол. Алкоголь также связывается с рецепторами ГАМК-А (GABA-A). GABA-B-рецепторы активируются баклофеном, используемым при лечении мышечного спазма.
Серотонин (5-гидрокситриптамин, или 5-НТ) синтезируется в ядре шва и нейронах средней линии моста и верхней части ствола мозга. Триптофан гидроксилируется гидроксилазой триптофана до 5-гидрокситриптофана, затем декарбоксилируется с образованием серотонина. Уровень серотонина регулируется интенсивностью захвата триптофана и внутриклеточной концентрацией фермента моноаминооксидазы (МАО), которая разрушает серотонин. В конечном итоге серотонин выводится с мочой в виде 5-гидроксииндоацетиловой кислоты, или 5-ГИАК.
Серотонинергические (5-НТ) рецепторы, которых на сегодня насчитывается по крайней мере 15 подтипов, подразделяют на 5-HT1 (4 подтипа), 5-HT2 и 5-HT3. Селективные агонисты серотониновых рецепторов (например, суматриптан) могут купировать приступы мигрени. Селективные ингибиторы обратного захвата серотонина (СИОЗС) также использоваться для лечения нескольких психических расстройств (например, депрессии, тревоги, обсессивно-компульсивного расстройства, посттравматического стрессового расстройства).
Ацетилхолин – основной нейромедиатор мотонейронов ствола головного мозга и спинного мозга, вегетативных преганглионарных волокон, постганглионарных холинергических (парасимпатических) волокон и многих нейронов в ЦНС (например, в базальных ганглиях, двигательных отделах коры головного мозга). Ацетилхолин синтезируется из холина и ацетил-коэнзима А с участием фермента ацетилхолинтрансферазы, его действие непродолжительно из-за локального гидролиза ацетилхолинэстеразой до холина и ацетогруппы. Уровень ацетилхолина регулируется активностью фермента ацетилхолинтрансферазы и количеством захватываемого холина. При болезни Альцгеймера уровень ацетилхолина снижается.
Холинергические рецепторы подразделяются на никотиновые N1 (мозговое вещество надпочечников и ганглии вегетативной нервной системы) или N2 (скелетная мускулатура) и мускариновые M1 – M5 (широко представлены в ЦНС). M1 экспрессируются в вегетативной нервной системе, полосатом теле, коре и гиппокампе; M2 – в вегетативной нервной системе, сердце, гладких мышцах кишечной стенки, заднем мозге (ствол и варолиев мост) и мозжечке.
Дофамин взаимодействует с рецепторами ряда периферических нервных волокон, но преимущественно – с центральными нейронами (в частности, нейронами черной субстанции, среднего мозга, передней части покрышки и гипоталамуса). Аминокислота тирозин захватывается дофаминергическими нейронами и преобразуется тирозингидроксилазой в 3,4-дигидроксифенилаланин (ДОФА), который декарбоксилируется декарбоксилазой ароматических l-аминокислот с образованием дофамина. После высвобождения и взаимодействия с рецепторами оставшийся дофамин подвергается активному обратному захвату в нервное окончание. Уровень дофамина в нервных окончаниях регулируется МАО (разрушающей дофамин) и тирозингидроксилазой.
Дофаминергические рецепторы подразделяются на D1 – D5. D3 и D4 задействованы в процессы контроля мышления (уменьшая выраженность негативных симптомов шизофрении); D2-рецепторы регулируют функции экстрапирамидной системы. Однако сродство к определенному типу рецепторов не позволяет предсказать функциональный ответ (внутреннюю активность). Например, у ропинирола, имеющего высокое сродство к D3-рецепторам, внутренняя активность проявляется активацией D2-рецепторов.
Норадреналин – нейромедиатор большинства постганглионарных симпатических волокон и многих центральных нейронов (например, в голубоватом пятне ретикулярной формации ствола и гипоталамусе). Его предшественник, тирозин, преобразуется в дофамин, который гидроксилируется дофамин-бета-гидроксилазой с образованием норадреналина. После высвобождения и взаимодействия с рецепторами часть норадреналина разлагается катехол-O-метилтрансферазой (КОМТ), а остаток подвергается активному обратному захвату в нервное окончание, где он разлагается под действием МАО. Внутринейронный уровень норадреналина регулируют ферменты тирозингидроксилазы, дофамин-бета-гидроксилазы и моноаминоксидазы (МАО).
Адренергические рецепторы подразделяют на альфа-1 (постсинаптические в симпатической нервной системе), альфа-2 (пресинаптические в симпатической нервной системе и постсинаптические в головном мозге), бета-1 (в сердце) или бета-2 (в других структурах, иннервируемых симпатической нервной системой).
Эта группа соединений представляет собой опиоиды.
Эндорфины – полипептиды, которые активизируют многие центральные нейроны (например, в гипоталамусе, оливах, таламусе и голубоватом пятне). Тело клетки содержит крупномолекулярный полипептид, называемый проопиомеланокортин, предшественник альфа-, бета- и гамма-эндорфинов. Проопиомеланокортин транспортируется по аксону и расщепляется на фрагменты; один из них – это бета-эндорфин, содержащийся в нейронах, расположенных в околоводопроводном сером веществе, структурах лимбической системы и крупных катехоламинсодержащих нейронах головного мозга. После высвобождения и взаимодействия с рецепторами бета-эндорфин подвергается гидролизу пептидазами.
Энкефалины включают в себя мет-энкефалин и лей-энкефалин – это низкомолекулярные пептиды, присутствующие во многих центральных нейронах (например, в сером веществе бледного шара, таламуса, хвостатого и центрального ядер). Их предшественник проэнкефалин образуется в теле клетки, затем расщепляется специфическими пептидазами до активных пептидов. Эти вещества также определяются в спинном мозге, где они действуют как нейромедиаторы сигналов боли. Нейромедиаторы сигналов боли в заднем роге спинного мозга – глутамат и субстанция Р. Энкефалины уменьшают количество высвобождаемого нейромедиатора и гиперполяризуют (придают больший отрицательный заряд) постсинаптическую мембрану, снижая образование потенциалов действия и восприятие боли на уровне постцентральной извилины. После высвобождения и взаимодействия с пептидергическими рецепторами энкефалины гидролизируются в меньшие, неактивные пептиды и аминокислоты. По причине быстрой инактивации экзогенных энкефалинов в организме их клиническое использование невозможно. В качестве анальгетиков применяют более устойчивые молекулы (например, морфин).
Рецепторы энкефалинов-эндорфинов (опиоидные) классифицируют на мю-1 и мю-2 (влияющие на сенсорно-двигательную интеграцию и анальгезию), дельта-1 и дельта-2 (влияющие на двигательную интеграцию, познавательные функции и анальгезию) и каппа-1, каппа-2 и каппа-3 (влияющие на регуляцию водного баланса, анальгезию и потребление пищи). Сигма-рецепторы, в настоящее время классифицируемые как неопиоидные, расположены преимущественно в гиппокампе и связываются с фенилциклидином. Новые данные предполагают наличие еще многих фармакологически значимых подтипов рецепторов. Компоненты молекулы предшественника белка-рецептора могут быть перестроены в ходе синтеза рецептора с образованием нескольких вариантов рецептора (например, 27 вариантов соединения мю-опиоидного рецептора). Кроме того, 2 рецептора могут объединиться (димеризация) с образованием нового рецептора.
Динорфины – группа из 7 пептидов со сходными аминокислотными последовательностями. Наряду с энкефалинами они относятся к опиоидам.
Субстанция Р – пептид, обнаруживаемый в центральных нейронах (ножке шишковидной железы – эпифиза, черной субстанции, базальных ганглиях, продолговатом мозге и гипоталамусе) и в высоких концентрациях – в ганглиях задних корешков. Интенсивные афферентные болевые стимулы индуцируют высвобождение субстанции Р. Последняя модулирует нейрональный ответ на боль и настроение; посредством активации NK1A-рецепторов, расположенных в стволе головного мозга, она регулирует такие эффекты, как тошнота и рвота.
Оксид азота (NО) – неустойчивое газообразное соединение, которое опосредует многие нейрональные процессы. Он образуется из аргинина при участии NO синтетазы. Нейромедиаторы, вызывающие повышение внутриклеточного содержания кальция (например, субстанция Р, глутамат, ацетилхолин), стимулируют синтез NО в нейронах, экспрессирующих NO-синтетазу. NО может выполнять функцию внутриклеточного мессенджера; он может диффундировать из клетки во второй нейрон и вызывать в нем физиологические реакции (например, долговременную потенциацию – усиление определенных пре- и постсинаптических ответов как один из механизмов обучения) или увеличивать глутаматную (NMDA) рецептор-опосредованную нейротоксичность (например, при болезни Паркинсона, инсульте или болезни Альцгеймера). NO влияет на другие нейромедиаторы (например, ГАМК и ацетилхолин), изменяя приток кальция в клетки для увеличения высвобождения других нейромедиаторов.
Дополнительные газообразные нейромедиаторы включают монооксид углерода (CO) и сероводород (H2S). Эти медиаторы вырабатываются в клетках по всему телу (включая головной мозг). Эндогенный CO образуется в результате метаболизма гема и может участвовать в процессах, связанных с развитием лихорадки, воспалением, выживанием клеток и контролем расширения кровеносных сосудов. Некоторые ферменты участвуют в продукции H2S, который, как полагают, необходим для формирования и сохранения воспоминаний.
Остается не до конца изученной роль еще многих потенциальных нейромедиаторов, в том числе гистамина, вазопрессина, вазоактивного кишечного пептида, карнозина, брадикинина, холецистокинина, бомбезина, соматостатина, рилизинг-фактора адренокортикотропного гормона, нейротензина и, возможно, аденозина.
Эндоканнабиноиды — это эндогенные нейромедиаторы на основе липидов, регулирующие работу мозга, эндокринной и иммунной систем.
В результате заболеваний либо воздействия веществ, способных нарушать синтез, высвобождение, взаимодействие с рецептором, распад или обратный захват нейромедиаторов, вызывать изменения количества и аффинности рецепторов развиваются неврологические или психические симптомы и заболевания (см. таблицу Примеры заболеваний, связанных с нарушениями нейротрансмиссии Примеры заболеваний, связанных с нарушениями нейротрансмиссии ). Препараты, вмешивающиеся в процесс нейротрансмиссии, могут облегчить течение многих из этих заболеваний (например, болезнь Паркинсона, депрессии).