Role of PNs in Pain Signaling
The Dorsal Horn and Ascending Pain Pathway
While it is widely appreciated that acute pain serves important biological functions, persistent or ongoing pain serves no apparent biological purpose, but has far-reaching impacts on patients and society. As for other sensory modalities, such as touch, heat/cold, and itch, we have a good understanding of the anatomy of the pathway over which noxious (or potentially painful) signals generated in skin, muscle, joints, and viscera travels to the brain via a series of synaptic connections on neurons located in various CNS regions or “pain nodes.” These nodes are located in anatomically discrete regions and, importantly, pain perception can be dramatically altered depending on the way an incoming sensory signal is processed (or passed on) at these nodes. Much effort has therefore focused on understanding how sensory signals are processed within the different nodes of the ascending pain pathway. This is especially the case for the first central node: i.e., the dorsal horn of the spinal cord. Here, signals carried on peripheral afferents combine with inputs from local interneurons (INs) and descending brainstem centers to determine whether information is relayed to higher brain centers. The reception of this information produces the sensory and emotional components of experience, we call pain (reviewed in more detail in: Todd, 2010; Peirs and Seal, 2016). The relay of nociceptive information from the spinal cord dorsal horn to higher brain centers is ultimately achieved by the output and axon of specialized neurons called projection neurons (PNs). This review focuses on what we believe is an overlooked element in dorsal horn pain processing, namely the role of PN axon collaterals that branch and terminate locally. These collaterals must share PN output with other dorsal horn neurons; however, their impact remains to be determined.
PN Anatomy, Projections, and Synaptic Inputs
As the sole output cell of the dorsal horn, PNs have long been recognized as a vital element in spinal pain processing. Classically, they are considered to reside in laminae I and IV–V of the dorsal horn, with superficial and deep PNs being involved in nociceptive specific signaling or more broadly tuned signals that span innocuous to noxious ranges (wide dynamic range), respectively (Christensen and Perl, 1970; Coghill et al., 1993; Craig, 2003; Wercberger and Basbaum, 2019). Recent work in rodents, whereby PNs are labeled via retrograde tracer injections in the brainstem and thalamus, have provided more detailed information on the location of PN somata in the dorsal horn. PNs are concentrated in lamina I and the lateral spinal nucleus, absent in lamina II, and scattered throughout deeper laminae III–VI (Al-Khater et al., 2008) and lamina X (Krotov et al., 2017). Importantly, PNs are not a frequently encountered cell type in the dorsal horn. They make up <5% of the neurons in laminae I, 1% of the neurons in the superficial dorsal horn (laminae I–II) and are only sparsely scattered in the deeper laminae (Spike et al., 2003; Polgar et al., 2010; Cameron et al., 2015). Their scarcity alone has made PNs difficult to study, and this has hindered our efforts to understand how they integrate with other dorsal horn circuits (Brown, 1982).
The axons of PNs that transmit cutaneous pain, along with thermal and itch modalities, leave the spinal cord by traveling ventrally, crossing to the contralateral cord within a few segments, and finally ascending in the anterolateral tract (Todd, 2017). Transmission of pain associated with deep structures (e.g., viscera) ascends to the brain in either the anterolateral tract or dorsal column pathways (Willis et al., 1999). Textbook accounts have the axons of PNs terminating in the thalamus before being relayed to somatosensory cortex and limbic structures where the pain percept and its emotional or effective responses are generated. While this holds true for primates, recent work in rodents, however, has provided evidence for extensive PN axon terminals in brain stem centers, such as the nucleus of the solitary tract, caudal ventrolateral medulla, parabrachial nucleus (PBN), and the periaqueductal gray (Al-Khater and Todd, 2009; Cameron et al., 2015).
PN Function in Pain Processing
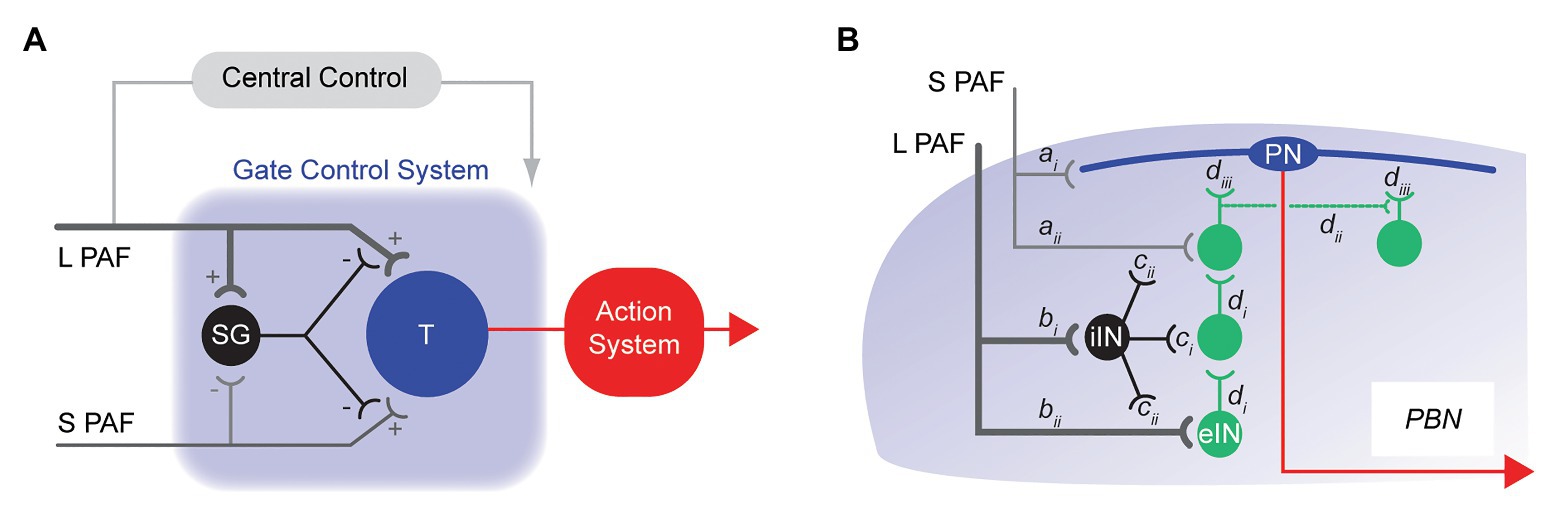
Our current understanding of how the spinal cord relays nociceptive signals from the dorsal horn to higher brain centers is still heavily influenced by the gate control theory of pain (Figure 1A) published in 1965 (Melzack and Wall, 1965). Although many of the fine details in this theory have since been refined and modified, at its heart is the premise that functional inhibition is critical for appropriate spinal sensory processing and normal pain perception (Yaksh, 1999; Zeilhofer et al., 2012; Mendell, 2014). Specifically, the gate control theory assigned inhibitory INs (iINs) a role in preventing touch inputs from activating pain circuits. More recently, a role for excitatory INs (eINs) in pathological pain has been added where polysynaptic pathways associated with touch information infiltrate nociceptive circuits (Neumann et al., 2008; Takazawa and MacDermott, 2010). Thus, IN networks in the dorsal horn are accepted as a critical factor in shaping output signals that are conveyed to the brain by PNs to produce pain. The final element identified in the original gate control theory is “central control,” where signals arising from the brain itself descend and modify spinal dorsal horn activity. Indeed, several brain structures are now well-established sources of descending input to the spinal dorsal horn (Suzuki et al., 2004; François et al., 2017; Lu et al., 2018). They have the capacity to facilitate or inhibit dorsal horn circuits and alter the gain of pain signaling in this region.
Figure 1. Historical models of spinal pain processing. (A), schematic shows the originally proposed circuitry for the Gate Control Theory of Pain. Touch related sensory information is relayed to the dorsal horn by large fiber (myelinated) primary afferents (L-PAF), whereas nociceptive inputs are relayed by small fiber (unmyelinated) primary afferents (S-PAF). The transmission cell (T) represents the output cell [projection neuron (PN)] of the dorsal horn. An inhibitory interneuron (iIN) is key to the model and is represented as SG. Activation of the SG cell by L-PAF suppresses T cell activation, thereby reducing (gating) pain signaling (i.e., action system). Alternatively, S-PAF activation inhibits SG cell activity, facilitating pain signaling output from the T cell (action system). (B), schematic summarizing more modern views of spinal pain processing circuits. Nociceptive information (S-PAF) is relayed into the superficial dorsal horn and terminates on lamina I PNs (ai) and local interneurons (aii), whereas touch related sensory information (L-PAF) terminates in the deep dorsal horn (bi and bii). Polysynaptic circuits of excitatory interneurons (eINs) circuits (di) provide a channel for L-PAF input to excite PNs in lamina I (diii). Excitatory interneurons also form polysynaptic networks (dii) that can enhance nociceptive signaling onto lamina I PNs. Populations of iINs also receive sensory signals from the periphery and suppress the activity of nociceptive and touch related circuits via: postsynaptic inhibition of these circuits, and presynaptic inhibition of sensory inputs (ci and cii, respectively). Supra-threshold excitation causes transmission of information along the PN axon (red line) to brainstem and midbrain structures, such as the parabrachial nucleus (PBN).
Building on the foundations established in gate control theory, our modern view of spinal sensory circuits in the dorsal horn still includes inhibitory gating mechanisms, with more recent transgenic technologies substantially advancing these views (Figure 1B). For example, termination zones are well-established for small diameter nociceptive primary afferents in the superficial dorsal horn and for large diameter tactile primary afferents in the deep dorsal horn (Peirs and Seal, 2016). We now know deep and superficial laminae are linked by polysynaptic circuits of eINs (Brown, 1982; Abraira et al., 2017). This provides a pathway for touch related sensory information to be relayed, or infiltrate, into lamina I and excite lamina I PNs, activating the ascending pain pathway. Populations of eINs have also been shown to form excitatory networks that support reverberating excitation in these circuits. Finally, iINs have been shown to act through a variety of connections to mediate presynaptic and postsynaptic inhibition and thus regulate, or gate, spinal sensory processing. In summary, our current understanding of how nociceptive signals are processed in the dorsal horn is built on the interaction of three distinct factors (sensory afferents, dorsal horn INs, and descending brain pathways). Together, the summed activity of these elements determines PN outputs that evoke the pain experience in the brain. We propose PN axon collaterals represent a missing fourth factor that must be incorporated into current models of spinal pain processing.
Axon Collateralisation in the Dorsal Horn of the Spinal Cord
The anatomy and function of PNs have been studied extensively for over 60 years (Wercberger and Basbaum, 2019) as they play such a key role in channeling highly processed information from the dorsal horn to supraspinal targets. This view is supported by several studies that show a dorsal flow of sensory signals through anatomically and functionally connected dorsal horn IN populations to PNs that can then relay this information to the brain (Cordero-Erausquin et al., 2009; Hachisuka et al., 2018; Smith et al., 2019). The fact that PNs project to readily accessed brainstem centers such as the PBN and periaqueductal gray has facilitated their identification and study in spinal cord slices through retrograde labeling approaches (Ruscheweyh et al., 2004; Dahlhaus et al., 2005). As a result, we now have some information on the discharge properties (Ruscheweyh et al., 2004), and involvement in certain forms of synaptic plasticity (Ikeda et al., 2006). Few studies have examined PN axon collaterals, even though recent data (see below) show they provide a substrate for pain signals destined for the brain to be shared with, or “copied to” circuitry within the spinal cord. The phenomenon termed efference copy in other systems (Sperry, 1950).
Anatomical Evidence for Axon Collaterals in the Dorsal Horn
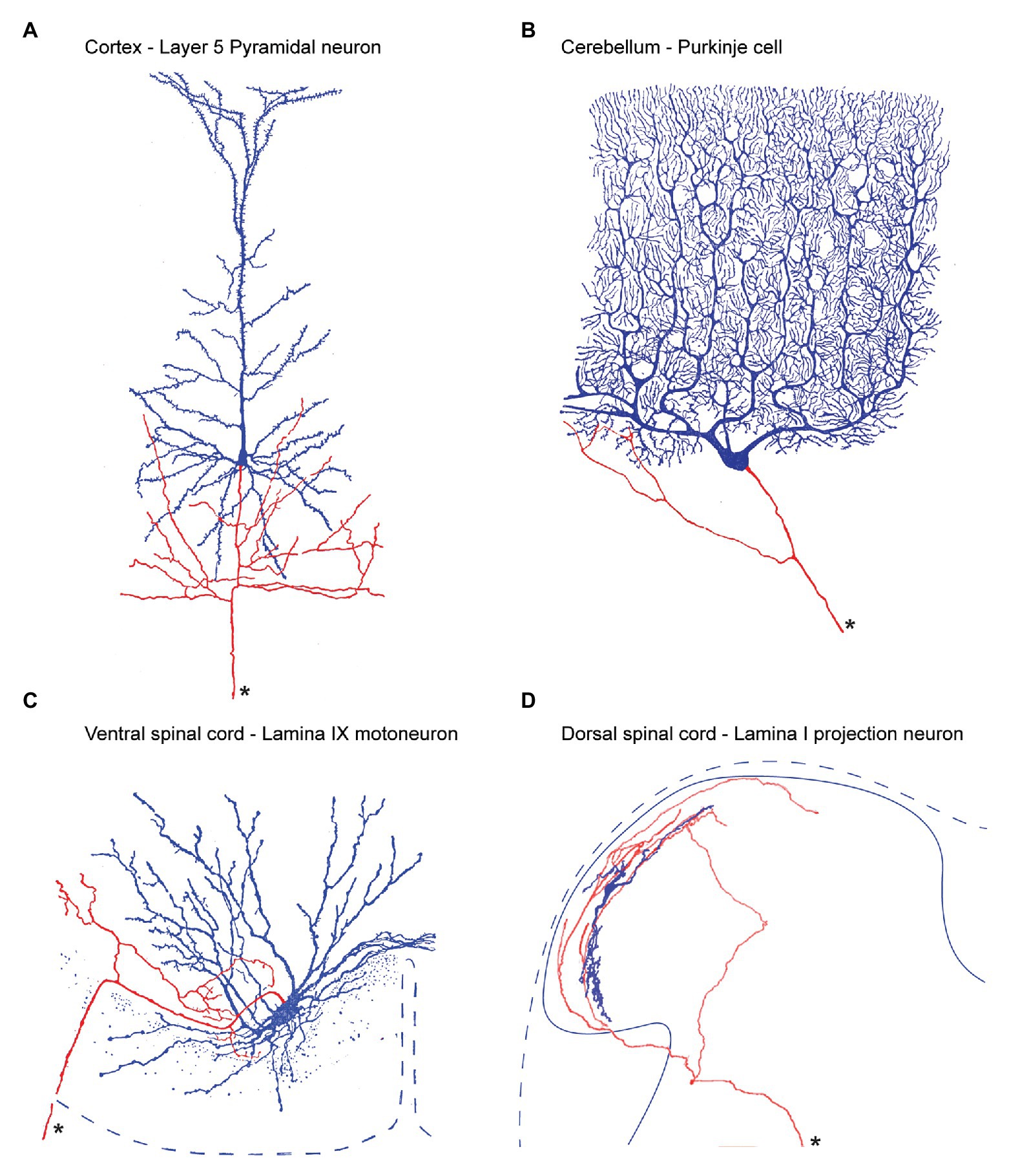
Local branches and collaterals arising from the axon of principle (output) neurons are a feature of many CNS regions, including the cortex, cerebellum, and ventral horn of the spinal cord (Figure 2). For dorsal horn PNs, most information we currently have on local axon collaterals comes from electrophysiological studies on identified PNs, where various labels are included in intracellular recording electrodes. Reconstructions of filled PNs have documented axon collaterals in monkey (Beal et al., 1981), cat (Bennett et al., 1981; Brown, 1981; Hylden et al., 1985, 1986; Maxwell and Koerber, 1986; Light et al., 1993), and rat (Luz et al., 2010; Szucs et al., 2010, 2013). Surprisingly, no data are yet available for PN axon collaterals in mouse, despite the increased use of genetically modified mice for pain studies.
Figure 2. Output neuron axon collateral anatomy throughout the central nervous system. (A), within the cerebral cortex, Layer 5 Pyramidal neurons provide the principle output which can project to regions as distant as the lumbar spinal cord, to neighboring cortical regions, or other brain regions such as the thalamus. In addition, Pyramidal axons branch locally producing an extensive local collateral network (soma and dendrites labeled blue, axon labeled red, and main axon marked by an asterisk). (B), Purkinje cells are the output cells of the cerebellar cortex and send axons to deep cerebellar nuclei. Purkinje cell axons also branch to produce a local collateral network (C), Motoneurons are the output cell of the ventral spinal cord. Their long axons exit the ventral spinal root and innervate skeletal muscle. In addition, motoneuron axons branch within the ventral horn to produce an extensive local collateral network. (D), Lamina I PNs are the output cell of the dorsal spinal cord. Their main axon crosses the midline and ascends to various regions including the PBN, and periaqueductal gray, and thalamus. Lamina I PNs also exhibit an extensive local collateral network. Panels (A–C) modified from (Cajal, 1952) and (D) is from (Szucs et al., 2010).
Szucs et al. (2010) have provided the most detailed characterization of PN collaterals within lamina I of the rat dorsal horn. They used an ex vivo intact spinal cord preparation (lumbosacral enlargement, L1–L6), which allows visualization and identification of presumptive PNs based on their superficial location, large size, and the post hoc tracing of filled-cell axons tracking to the anterolateral tract. Notably, data using this approach showed PN axon collateral territories were extensive and confined to the ipsilateral cord. PN axon collaterals could be classified into four types according to their course and territory in the dorsal horn. Dorsal collaterals ramified extensively within laminae I–IV of the dorsal horn gray matter and sometimes entered Lissauer’s tract. Ventral collaterals projected into the propriospinal and ventral motor territories (Flynn et al., 2011). Lateral collaterals ran primarily in the rostrocaudal plane for about a spinal segment. Finally, mixed collaterals exhibited combinations of the other three types. Importantly, in all four types, en-passant and terminal synaptic boutons were observed on PN axon collaterals – implying the potential for local (spinal) signaling. The authors concluded that PN axon collaterals likely have an important function in local circuits including intra- and intersegmental spinal cord processing. Furthermore, this widespread distribution positions the ascending signals carried by PN collaterals to influence the spinal circuits that encode pain, itch, touch, visceral pain, as well as proprioception and motor output.
Neurochemical Phenotype and Function of PN Axon Collaterals
The Todd group (Cameron et al., 2015) showed via retrograde labeling and immunohistochemistry that 97% of the synaptic boutons on PN axons in the PBN expressed VGLUT2. This matches the expected excitatory nature of PNs. Presumably, this would also apply to the en passant synaptic boutons on PN collaterals within the spinal cord. vGLUT2 is also detected in the majority (>85%) of the output cells in the medullary dorsal horn (Ge et al., 2010; Zhang et al., 2018). Assuming conservation between the spinal and brainstem dorsal horns, these observations further support the likelihood that spinal cord PN collaterals mediate excitatory actions on their immediate, local targets. While the case for glutamate signaling is clear, this work does not exclude the potential for PN terminals to also release neurotransmitters other than glutamate. For example, the same work that confirmed VGLUT2 expression in PN axons also reported some terminals expressed Substance P (~16%). Furthermore, precedent for co-transmission can be found in the ventral horn of the spinal cord, where motoneurons have been shown to utilize multiple neurotransmitters (acetylcholine and glutamate) at synapses in their axon collaterals that excite Renshaw cells (Renshaw, 1946; Callister and Graham, 2010; Lamotte d’Incamps et al., 2017; Callister et al., 2020). Thus, the available anatomical data suggest extensively ramified PN axon collaterals can make excitatory synaptic connections with neurons in the dorsal, intermediate, and ventral horn; however, the functional role of additional transmitters (e.g., peptides) remains to be established.
To the best of our knowledge, there is only one demonstration of a functional synaptic connection made by a PN axon collateral within dorsal horn, albeit from a putative PN in the young rat spinal cord. In this example, Luz et al. (2010) used paired patch clamp electrophysiology and recorded a monosynaptic excitatory connection between two putative PNs. It was not reported if the connection was strong enough to generate a spike in the post-synaptic PN; however, inputs from other lamina I INs were capable of generating spikes in PNs. These data, coupled with the anatomical data presented above, strongly suggest PN axon collaterals have an active role in the dorsal horn of the spinal cord. Substantially, more information will be required; however, before PN axon collateral signaling can be incorporated into models of spinal sensory processing.
Axon Collateral Function in Other CNS Regions
Since the time of Cajal, neuroscientists have found it useful to organize the elements that make up various CNS regions into three components: afferent inputs that bring information to a region, INs that are involved in local processing, and principal/relay/output or PNs that transmit processed signals. The later sends out a long axon that carries information to another CNS region or peripheral target. This model also acknowledges a role for local collaterals arising from output neurons (e.g., “the principal or output neuron can also take part in local processing and does so by axon collaterals that ramify extensively among local circuit neurons” Shepherd, 2004).
While the roles of dorsal horn PN axon collaterals remains unknown, the function of such recurrent circuitry has been clarified within other CNS regions. For example, the Schaffer-collateral system in hippocampus, composed of axon collaterals of CA3 pyramidal cells, forms an integral part of the trisynaptic pathway, and the synapses they form onto CA1 pyramidal cells are the most widely studied synaptic connections of any within the central nervous system (Freund and Buzsáki, 1996). In the following section, we discuss some of these PN-derived feedback circuits, and by highlighting common motifs among these examples, provide insight into the potential functions within the spinal dorsal horn.
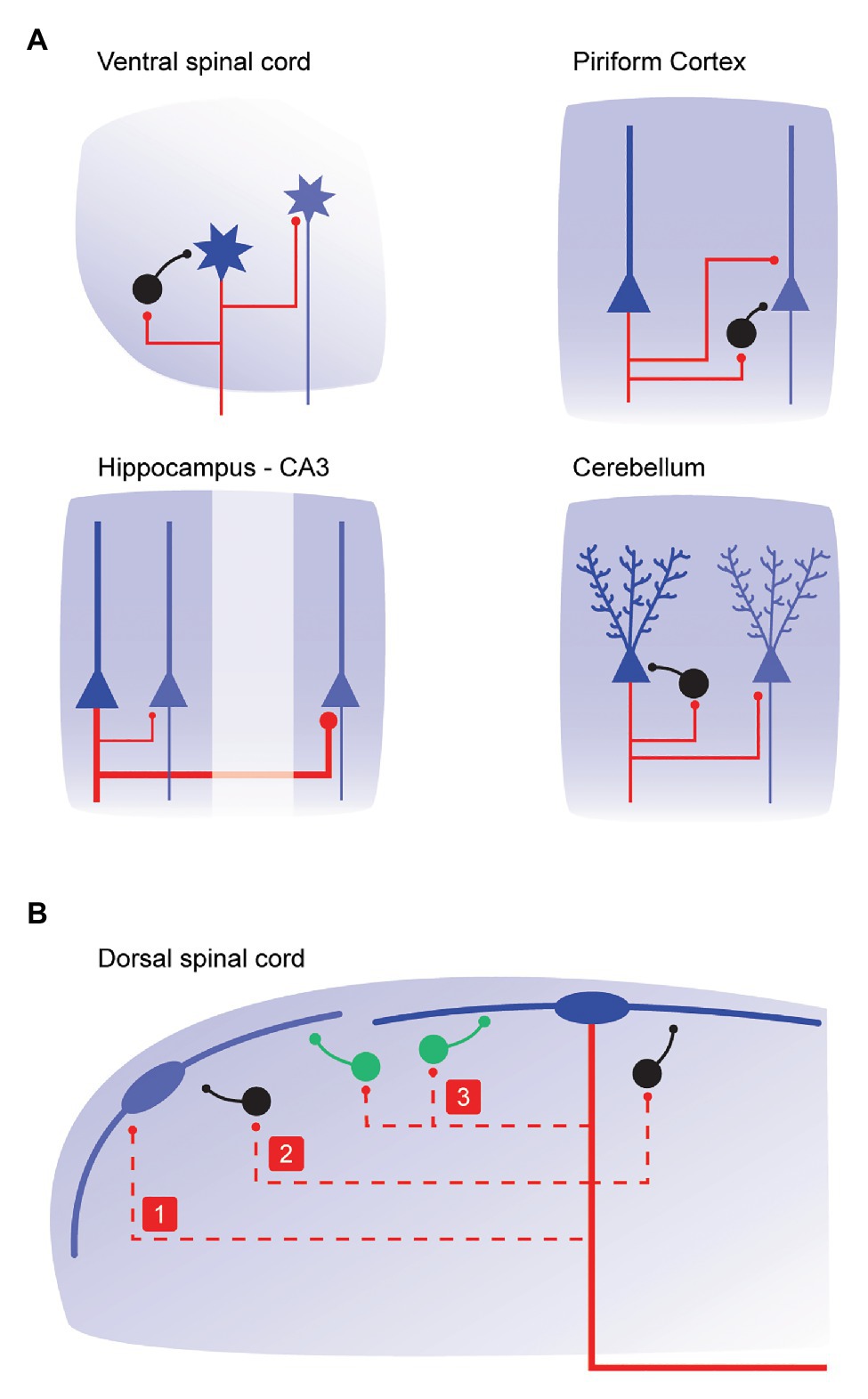
Our best understood example of axon collateral function in the spinal cord stems from studies of “recurrent inhibition” in the ventral horn of the spinal cord (Figure 3A). As early as the 1940s, there was compelling anatomical evidence for the existence of motoneuron axon collaterals. Importantly, these collaterals terminated in the vicinity of other ventral horn cells. The function of this collateral system was initially studied by Birdsey Renshaw in a series of experiments over 1938–1941 (see Callister et al., 2020). Renshaw showed that “reflex” motoneuron activity, initiated by stimulating dorsal roots or dorsal columns, was inhibited by stimulating cut ventral roots (Renshaw, 1941). He proposed that motoneuron axon collaterals produced inhibition in the ventral horn. Eccles subsequently studied the important inhibitory neuron that was underpinning the observation, termed the Renshaw cell (Eccles et al., 1954). It represents one of the first neural circuits ever described in the CNS, and by extension the first to involve axon collateral signaling.
Figure 3. Connectivity and function of local axon collateral networks throughout the central nervous system. (A), schematics summarizing axon collateral connectivity in CNS regions where their function is well-characterized. Primary output neurons in each region are shown in blue, the axons and collaterals from these cells are shown in red, and local iINs are black. Local axon collaterals arising from motoneurons in the ventral horn (upper left) contact inhibitory Renshaw cells and neighboring motoneurons. Functionally, these connections are implicated in varying force and in rapidly increasing force, respectively. In the piriform cortex (upper right), local axon collaterals arising from pyramidal neurons contact local iINs and other pyramidal interneurons. These connections are critical for stable invariant odor coding regardless of concentration, and recruitment of stable populations of Pyramidal neuron including cells that may not receive primary odor inputs. In the CA3 region of the hippocampus (lower left), pyramidal neuron axon collaterals contact other pyramidal neurons with a distal to proximal density (axon collateral thickness is proportional to synaptic drive). This allows the two regions to serve different roles. The collateral innervation of more proximal CA3 neurons is crucial for memory storage (pattern recognition), whereas distal CA3 contacts are important for memory retrieval (pattern completion). Finally, Purkinje cell axon collaterals in the cerebellum (lower right) contact local iINs and other Purkinje cells to provide inhibitory feedback and form feedforward loops. These are important for restricting local activity to the cerebellum’s well-defined parasagittal zones. (B), schematic shows local axon collateral connections (red dashed lines) that could arise from lamina I dorsal horn PNs (blue). Based on collateral connectivity summarized in (A), PN collaterals in the dorsal horn may contact: (1) neighboring PNs; (2) local iINs; or (3) local excitatory interneurons (green). These connections may be relevant for shaping intensity, receptive field properties, and the modality of PN output that is ultimately relayed to the brain.
In its simplest form, activation of the motoneuron and its axon collateral, results in the recruitment of the Renshaw cells. In turn, these Renshaw cells then inhibit the homonymous motoneuron pool with glycinergic inhibition. This feedback is not trivial, and evidence has shown that input from one Renshaw cell can cease activity in its coupled motoneuron (Bhumbra et al., 2014). This coupling arrangement has been viewed as a variable gain regulator that allows muscles to produce a wide range of contractile forces (Moore et al., 2015). It is also thought to be important in preventing the runaway excitation of the motoneuron, acting to enable smooth motor control and prevent muscle spasticity such as in Clostridium Tetani infection (tetanus). More recently, motoneuron axon collaterals have been shown to target neighboring motoneuron (Spike et al., 2003; Bhumbra and Beato, 2018). Collateral input is to both local (intrasegmental) and more distal (intersegmental) motoneurons and is thought to play a role in progressively recruiting motor neurons to rapidly increase muscle force. As previously noted, PN collaterals in the dorsal horn are similarly arranged in both inter- and intrasegmental territories. This suggests they could provide recurrent inhibition to PNs as well as recruiting neighboring PNs. The capacity of the motoneuron circuit to both alter signaling range and rapidly increase the intensity of ventral horn outputs implies PN axon collaterals may help tune the boundaries of sensation and the intensity of pain signals that are ultimately transmitted to the brain.
In the brain, output neurons in the cerebral cortex, hippocampus and amygdala also give rise to extensive local axon collaterals and, in these regions, much is also known about function. In the olfactory (piriform) cortex, axon collaterals form a sparse excitatory network among output “pyramidal” neurons (Figure 3A). This connectivity is thought to allow odors to recruit ensembles of pyramidal neurons including cells that do not directly receive an odor input (Franks et al., 2011). Pyramidal neuron collaterals also activate feedforward and feedback inhibition, via local INs. The latter is critical for stable “invariant” odor coding, regardless of changes in odor concentration (Bolding and Franks, 2018). In the basolateral nucleus of the amygdala, principal cell collaterals show spatial selectivity whereby iINs are contacted by terminals on proximal collaterals, and, other principal cells are contacted by those on more distal collaterals (Duvarci and Pare, 2014). This configuration is considered important to prevent runaway excitation within the primary cell, while allowing associative interactions with more distal principal cell populations that underpin associative conditioning (such as fear). In the hippocampus, the Schaffer-collateral system plays a critical in memory processing (Figure 3A). Specifically, graded proximal to distal collateral density along CA3 allows proximal CA3 to perform important roles in responding to novel cues with a tendency to remap and store new memories (i.e., as in pattern recognition). Alternatively, distal CA3 with extensive collaterals is thought to drive memory retrieval functions (pattern completion), especially with degraded or incomplete input patterns (Lee et al., 2015). A similar associative excitatory collateral network has also been described for grid cells in medial entorhinal cortex. This is thought to be important for the correct neural representation of space (Couey et al., 2013). Extending these observations to spinal sensory processing in the dorsal horn, a similar excitatory collateral network connecting PNs, coupled with collateral connectivity to iINs could easily play a role in the reliable representation of sensory signals from the body surface (i.e., receptive fields). Furthermore, in terms of pain signaling, this arrangement would allow for receptive field expansion as observed following tissue damage (Figure 3B).
A final example of collateral signaling highlights that these output neuron configurations are not always excitatory. In the cerebellar cortex, the major output neuron, the Purkinje cell, is inhibitory. Various models of cerebellar function have existed for years (Eccles et al., 1967) based on a feedforward circuit with synaptic activity flowing from mossy fibers through granules cells to the Purkinje cell. These neurons have an extensive axon collateral system that is organized preferentially in the parasagittal plane (Watt et al., 2009). Recent advances have allowed detailed functional investigation of Purkinje cell collaterals in adult rodents. Witter et al., 2016, have shown these collaterals provide inhibitory feedback to several classes of INs and also contact neighboring Purkinje cells (Witter et al., 2016). These important feedback loops are considered important for regulating activity in the cerebellum’s well-known parasagittal zones. Thus, even when collaterals arise from inhibitory population’s they have been shown to play a role in delineating functional borders and confining excitation.
In summary, there are precedents for axon collaterals playing important roles in the function of various CNS regions via either excitation or inhibition (Figure 3A). Generally, these output neuron collaterals drive feedback inhibition through local INs or have amplifier and associative functions via feedforward excitation. Such data are not yet available for PN axon collaterals, however, insights from other collateral systems throughout the CNS suggest that new information on PN axon collaterals will have a major impact on the way we understand spinal sensory processing (Figure 3B).
New Techniques and a New Approach to Study PN Axon Collaterals
Two major factors have likely hampered our understanding of PN axon collateral signaling in the dorsal horn, compared to the relatively advanced understanding of collateral signaling in other regions. First, the scarcity of PNs in the dorsal horn (~1% of lamina I–II neurons vs. 70–90% principle neurons in cortex, hippocampus, and amygdala) makes them difficult to target with a microelectrode. Second, a definitive genetic characteristic or “signature” that distinguishes PNs from other dorsal horn cells remains to be identified. This contrasts with ventral horn motoneurons, for example, that can be easily identified by location (Lamina IX) and cholinergic markers.
A series of recent technical advances now permit progress in understanding the role PN axon collaterals in spinal sensory processing circuits. Specifically, viral gene transduction with specific trafficking and tropism properties allows gene targeting and protein expression to be directed to neuronal populations according to where their axons ultimately project. This is similar to the classical retrograde labeling approaches that involved injection of tracers, such as HRP, WGA, fast blue, and fluorescent microspheres, into brain regions, such as PBN, periaqueductal gray, thalamus, or rostroventromedial medulla. Application of modern gene targeting and protein expression approaches results in robust expression of fluorescent proteins (e.g., GFP, mCherry, and TdTomato). This allows visualization of dendritic and axonal processes to an extent not possible using classical tracers. Furthermore, multi-labeling experiments using brainbow constructs, a genetic cell-labeling technique that identifies individual cells with unique color hues (Weissman and Pan, 2015), will allow mapping of the relationship between populations of dorsal horn PNs in great detail.
Viral approaches also present an opportunity to express proteins that allow control of PN activity via optogenetic or chemogenetic techniques, both in vitro and in vivo. These methods are particularly relevant to our efforts to study PN axon collateral function in the dorsal horn. For example, channelrhodopsin-2 assisted circuit mapping (CRACM) could be achieved by selective photostimulation of PNs in acutely prepared tissue slices. The CRACM approach has been used to functionally characterize and map axon collateral connections of semilunar cells (a specific type of principle/output neuron) in piriform cortex. Optogenetic activation of semilunar cells produced recurrent excitation of collaterals that contacted a different population of output cells, termed superficial cells (Choy et al., 2017). CRACM has also been used to study the targets of Purkinje cell axon collaterals in the cerebellum. Notably, optogenetically identified connections contacted other Purkinje cells, molecular layer INs, and Lugaro INs, but not Golgi INs (Witter et al., 2016). These results highlight how the optogenetic approach can uncover functional collateral connectivity patterns that would take years to acquire using the low-yield and technically demanding paired patch clamp recording approach.
Transgenic manipulations that silence synaptic function have also been applied while using in vitro slice electrophysiology, as well as in anesthetized and freely behaving animals to study local axon collateral function. For example, work in the piriform cortex has used transgenic expression of tetanus toxin light chain (TeLC) to silence pyramidal cell axon collateral synapses while retaining the intrinsic excitability of these cells (Bolding and Franks, 2018). This approach confirmed local collateral signaling that recruited feedback iINs was critical for tuning the local response to concentration-invariant coding of odors. The same approach has also been used to silence the recurrent excitatory circuits of CA3 pyramidal neurons and assess the collateral network’s role in epilepsy (Yu et al., 2016). This manipulation reduced kainic acid-induced seizure activity, hippocampal epileptiform oscillatory activity, and cFos expression. This confirmed the long-held view that CA3 pyramidal neurons, and their extensive axon collateral networks, are critical for kainic-acid triggered seizures. These two examples highlight how transgenic targeting of axons and synaptic function allows axon collateral function to be comprehensively studied. Similar approaches in the dorsal horn may help clarify the importance of local PN axon collaterals in sensory experience, although the anatomy of the nociceptive pathway does present some challenges. Specifically, TeLC silencing would prevent local collateral signaling as well as silencing the ascending connections that rely nociceptive signals to the brain. Thus, it may be difficult to attribute any behavioral phenotype to a specific connection type. Despite this, the proximity of local collateral synapses to the PN cell body, versus the distant projections synapsing in the brain, may be advantageous. This could open a window whereby high local (spinal) TeLC expression achieves local silencing, before significant TeLC expression reaches the more distal brain connections. This delay could allow the direct assessment of PN derived recurrent feedback in the dorsal horn while maintaining normal neuronal excitability and upstream transmission of nociceptive signals.
Conclusion and Future Directions
The literature reviewed above provides clear evidence that a local axon collateral system exists in the spinal dorsal horn arising from its output cell, the PN. The only functional information on PN axon collaterals in the dorsal horn comes from a single observation at a connection between two putative PNs in tissue from a young animal. No other functional information is available on these connections. A more advanced understanding of local axon collateral function in other CNS regions suggests “feedforward” excitation of other PNs, and recurrent “feedback” inhibition through connections with iINs is likely to exist. Fortunately, the experiments required to clarify these proposed roles are now possible because of new transgenic and viral techniques that can be applied in the mouse. Accordingly, we suggest the following pressing questions can and need to be answered:
1. Do mouse dorsal horn PNs exhibit branching and local axon collaterals? Anatomical evidence for this and the existence of synaptic specializations has been provided in other species, but not mouse.
2. Do dorsal horn PNs that reside outside laminae I give rise to collateral systems and are they similar? The most detailed characterization, available in rat, only reported on axon collaterals arising from superficial lamina I PNs that could be visualized in an ex vivo intact spinal cord preparation.
3. Which type of dorsal horn neuron do PN axon collaterals target? As outlined above, three broad dorsal horn populations include PNs, eINs, and iINs.
As answers to these questions become available it will be possible to incorporate PN axon collateral signaling into models of spinal sensory processing and thereby include an important new player in these circuits. While it is not yet possible to definitively predict how this information will change our understanding of spinal pain processing, available evidence from other output neurons suggests sharing the ascending “output” pain signal with local spinal pain circuits will be important. This information needs to be first collected under naïve uninjured conditions. Future experiments can then ask whether dysfunctional collateral signaling exists in pain models (both neuropathic and inflammatory). Finally, if this detailed information identifies a discrete post-synaptic arrangement of PN axon collaterals, for example capable of blunting pain signals (such as the Renshaw cell), it will represent an attractive foundation from which to develop targeted, and selective new pain therapies.
Author Contributions
All authors contributed equally to all planning, writing and editing associated with this invited submission to a Frontiers Research Topic.
Funding
This work was funded by the National Health and Medical Research Council (NHMRC) of Australia (grants 631000, 1043933, 1144638, and 1184974 to BG and RC), the Biotechnology and Biological Sciences Research Council (BB/P007996/1 to DH), and the Hunter Medical Research Institute (grant to BG and RC). TB is supported by a scholarship from Glenn Moss through the Hunter Medical Research Institute.
Conflict of Interest
The authors declare that the research was conducted in the absence of any commercial or financial relationships that could be construed as a potential conflict of interest.
References
Abraira, V. E., Kuehn, E. D., Chirila, A. M., Springel, M. V., Toliver, A. A., Zimmerman, A. L., et al. (2017). The cellular and synaptic architecture of the mechanosensory dorsal horn. Cell 168, 295.e19–310.e19. doi: 10.1016/j.cell.2016.12.010
PubMed Abstract | CrossRef Full Text | Google Scholar
Al-Khater, K. M., Kerr, R., and Todd, A. J. (2008). A quantitative study of spinothalamic neurons in laminae I, III, and IV in lumbar and cervical segments of the rat spinal cord. J. Comp. Neurol. 511, 1–18. doi: 10.1002/cne.21811
PubMed Abstract | CrossRef Full Text | Google Scholar
Al-Khater, K. M., and Todd, A. J. (2009). Collateral projections of neurons in laminae I, III, and IV of rat spinal cord to thalamus, periaqueductal gray matter, and lateral parabrachial area. J. Comp. Neurol. 515, 629–646. doi: 10.1002/cne.22081
PubMed Abstract | CrossRef Full Text | Google Scholar
Beal, J. A., Penny, J. E., and Bicknell, H. R. (1981). Structural diversity of marginal (lamina I) neurons in the adult monkey (Macaca mulatta) lumbosacral spinal cord: a golgi study. J. Comp. Neurol. 202, 237–254. doi: 10.1002/cne.902020209
PubMed Abstract | CrossRef Full Text | Google Scholar
Bennett, G. J., Abdelmoumene, M., Hayashi, H., Hoffert, M. J., and Dubner, R. (1981). Spinal cord layer I neurons with axon collaterals that generate local arbors. Brain Res. 209, 421–426. doi: 10.1016/0006-8993(81)90164-5
PubMed Abstract | CrossRef Full Text | Google Scholar
Bhumbra, G. S., Bannatyne, B. A., Watanabe, M., Todd, A. J., Maxwell, D. J., Beato, M., et al. (2014). The recurrent case for the renshaw cell. J. Neurosci. 34, 12919–12932. doi: 10.1523/JNEUROSCI.0199-14.2014
PubMed Abstract | CrossRef Full Text | Google Scholar
Bhumbra, G. S., and Beato, M. (2018). Recurrent excitation between motoneurones propagates across segments and is purely glutamatergic. PLoS Biol. 16:e2003586. doi: 10.1371/journal.pbio.2003586
PubMed Abstract | CrossRef Full Text | Google Scholar
Cajal, S. R. (1952). Histologie du systeme nerveux de le’homme and des vertebres. Madrid: Intstituto Ramon Y Cajal.
Google Scholar
Callister, R. J., Brichta, A. M., Schaefer, A. T., Graham, B. A., and Stuart, D. G. (2020). Pioneers in CNS inhibition: 2. Charles Sherrington and John Eccles on inhibition in spinal and supraspinal structures. Brain Res. 1734:146540. doi: 10.1016/j.brainres.2019.146540
PubMed Abstract | CrossRef Full Text | Google Scholar
Cameron, D., Polgár, E., Gutierrez-Mecinas, M., Gomez-Lima, M., Watanabe, M., and Todd, A. J. (2015). The organisation of spinoparabrachial neurons in the mouse. Pain 156, 2061–2071. doi: 10.1097/j.pain.0000000000000270
PubMed Abstract | CrossRef Full Text | Google Scholar
Choy, J. M. C., Suzuki, N., Shima, Y., Budisantoso, T., Nelson, S. B., and Bekkers, J. M. (2017). Optogenetic mapping of intracortical circuits originating from semilunar cells in the piriform cortex. Cereb. Cortex 27, 589–601. doi: 10.1093/cercor/bhv258
PubMed Abstract | CrossRef Full Text | Google Scholar
Christensen, B. N., and Perl, E. R. (1970). Spinal neurons specifically excited by noxious or thermal stimuli: marginal zone of the dorsal horn. J. Neurophysiol. 33, 293–307. doi: 10.1152/jn.1970.33.2.293
PubMed Abstract | CrossRef Full Text | Google Scholar
Coghill, R. C., Mayer, D. J., and Price, D. D. (1993). Wide dynamic range but not nociceptive-specific neurons encode multidimensional features of prolonged repetitive heat pain. J. Neurophysiol. 69, 703–716. doi: 10.1152/jn.1993.69.3.703
PubMed Abstract | CrossRef Full Text | Google Scholar
Cordero-Erausquin, M., Allard, S., Dolique, T., Bachand, K., Ribeiro-da-Silva, A., and De Koninck, Y. (2009). Dorsal horn neurons presynaptic to lamina I spinoparabrachial neurons revealed by transynaptic labeling. J. Comp. Neurol. 517, 601–615. doi: 10.1002/cne.22179
PubMed Abstract | CrossRef Full Text | Google Scholar
Couey, J. J., Witoelar, A., Zhang, S. J., Zheng, K., Ye, J., Dunn, B., et al. (2013). Recurrent inhibitory circuitry as a mechanism for grid formation. Nat. Neurosci. 16, 318–324. doi: 10.1038/nn.3310
PubMed Abstract | CrossRef Full Text | Google Scholar
Dahlhaus, A., Ruscheweyh, R., and Sandkuhler, J. (2005). Synaptic input of rat spinal lamina I projection and unidentified neurones in vitro. J. Physiol. 566, 355–368. doi: 10.1113/jphysiol.2005.088567
PubMed Abstract | CrossRef Full Text | Google Scholar
Eccles, J. C., Fatt, P., and Koketsu, K. (1954). Cholinergic and inhibitory synapses in a pathway from motor-axon collaterals to motoneurones. J. Physiol. 126, 524–562. doi: 10.1113/jphysiol.1954.sp005226
PubMed Abstract | CrossRef Full Text | Google Scholar
Eccles, J. C., Ito, M., and Szentagothai, J. (1967). The cerebellum as a neuronal machine. New York: Springer-Verlag.
Google Scholar
Flynn, J. R., Graham, B. A., Galea, M. P., and Callister, R. J. (2011). The role of propriospinal interneurons in recovery from spinal cord injury. Neuropharmacology 60, 809–822. doi: 10.1016/j.neuropharm.2011.01.016
PubMed Abstract | CrossRef Full Text | Google Scholar
François, A., Low, S. A., Sypek, E. I., Christensen, A. J., Sotoudeh, C., Beier, K. T., et al. (2017). A brainstem-spinal cord inhibitory circuit for mechanical pain modulation by GABA and enkephalins. Neuron 93, 822.e826–839.e826. doi: 10.1016/j.neuron.2017.01.008
PubMed Abstract | CrossRef Full Text | Google Scholar
Franks, K. M., Russo, M. J., Sosulski, D. L., Mulligan, A. A., Siegelbaum, S. A., and Axel, R. (2011). Recurrent circuitry dynamically shapes the activation of piriform cortex. Neuron 72, 49–56. doi: 10.1016/j.neuron.2011.08.020
PubMed Abstract | CrossRef Full Text | Google Scholar
Ge, S. N., Ma, Y. F., Hioki, H., Wei, Y. Y., Kaneko, T., Mizuno, N., et al. (2010). Coexpression of VGLUT1 and VGLUT2 in trigeminothalamic projection neurons in the principal sensory trigeminal nucleus of the rat. J. Comp. Neurol. 518, 3149–3168. doi: 10.1002/cne.22389
PubMed Abstract | CrossRef Full Text | Google Scholar
Hachisuka, J., Omori, Y., Chiang, M. C., Gold, M. S., Koerber, H. R., and Ross, S. E. (2018). Wind-up in lamina I spinoparabrachial neurons: a role for reverberatory circuits. Pain 159, 1484–1493. doi: 10.1097/j.pain.0000000000001229
PubMed Abstract | CrossRef Full Text | Google Scholar
Hylden, J. L., Hayashi, H., Bennett, G. J., and Dubner, R. (1985). Spinal lamina I neurons projecting to the parabrachial area of the cat midbrain. Brain Res. 336, 195–198. doi: 10.1016/0006-8993(85)90436-6
PubMed Abstract | CrossRef Full Text | Google Scholar
Hylden, J. L., Hayashi, H., Dubner, R., and Bennett, G. J. (1986). Physiology and morphology of the lamina I spinomesencephalic projection. J. Comp. Neurol. 247, 505–515. doi: 10.1002/cne.902470410
PubMed Abstract | CrossRef Full Text | Google Scholar
Ikeda, H., Stark, J., Fischer, H., Wagner, M., Drdla, R., Jäger, T., et al. (2006). Synaptic amplifier of inflammatory pain in the spinal dorsal horn. Science 312, 1659–1662. doi: 10.1126/science.1127233
PubMed Abstract | CrossRef Full Text | Google Scholar
Krotov, V., Tokhtamysh, A., Kopach, O., Dromaretsky, A., Sheremet, Y., Belan, P., et al. (2017). Functional characterization of lamina X neurons in ex-vivo spinal cord preparation. Front. Cell. Neurosci. 11:342. doi: 10.3389/fncel.2017.00342
PubMed Abstract | CrossRef Full Text | Google Scholar
Lamotte d’Incamps, B., Bhumbra, G. S., Foster, J. D., Beato, M., and Ascher, P. (2017). Segregation of glutamatergic and cholinergic transmission at the mixed motoneuron Renshaw cell synapse. Sci. Rep. 7:4037. doi: 10.1038/s41598-017-04266-8
PubMed Abstract | CrossRef Full Text | Google Scholar
Lee, H., Wang, C., Deshmukh, S. S., and Knierim, J. J. (2015). Neural population evidence of functional heterogeneity along the CA3 transverse axis: pattern completion versus pattern separation. Neuron 87, 1093–1105. doi: 10.1016/j.neuron.2015.07.012
PubMed Abstract | CrossRef Full Text | Google Scholar
Light, A. R., Sedivec, M. J., Casale, E. J., and Jones, S. L. (1993). Physiological and morphological characteristics of spinal neurons projecting to the parabrachial region of the cat. Somatosens. Mot. Res. 10, 309–325. doi: 10.3109/08990229309028840
PubMed Abstract | CrossRef Full Text | Google Scholar
Lu, Y., Doroshenko, M., Lauzadis, J., Kanjiya, M. P., Rebecchi, M. J., Kaczocha, M., et al. (2018). Presynaptic inhibition of primary nociceptive signals to dorsal horn lamina I neurons by dopamine. J. Neurosci. 38, 8809–8821. doi: 10.1523/JNEUROSCI.0323-18.2018
PubMed Abstract | CrossRef Full Text | Google Scholar
Luz, L. L., Szucs, P., Pinho, R., and Safronov, B. V. (2010). Monosynaptic excitatory inputs to spinal lamina I anterolateral-tract-projecting neurons from neighbouring lamina I neurons. J. Physiol. 588, 4489–4505. doi: 10.1113/jphysiol.2010.197012
PubMed Abstract | CrossRef Full Text | Google Scholar
Maxwell, D. J., and Koerber, H. R. (1986). Fine structure of collateral axons originating from feline spinocervical tract neurons. Brain Res. 363, 199–203. doi: 10.1016/0006-8993(86)90680-3
PubMed Abstract | CrossRef Full Text | Google Scholar
Moore, N. J., Bhumbra, G. S., Foster, J. D., and Beato, M. (2015). Synaptic connectivity between renshaw cells and motoneurons in the recurrent inhibitory circuit of the spinal cord. J. Neurosci. 35, 13673–13686. doi: 10.1523/JNEUROSCI.2541-15.2015
PubMed Abstract | CrossRef Full Text | Google Scholar
Neumann, S., Braz, J. M., Skinner, K., Llewellyn-Smith, I. J., and Basbaum, A. I. (2008). Innocuous, not noxious, input activates PKCgamma interneurons of the spinal dorsal horn via myelinated afferent fibers. J. Neurosci. 28, 7936–7944. doi: 10.1523/JNEUROSCI.1259-08.2008
PubMed Abstract | CrossRef Full Text | Google Scholar
Polgar, E., Wright, L. L., and Todd, A. J. (2010). A quantitative study of brainstem projections from lamina I neurons in the cervical and lumbar enlargement of the rat. Brain Res. 1308, 58–67. doi: 10.1016/j.brainres.2009.10.041
PubMed Abstract | CrossRef Full Text | Google Scholar
Renshaw, B. (1941). Influence of discharge of motoneurons upon excitation of neighboring motoneurons. J. Neurophysiol. 4, 167–183. doi: 10.1152/jn.1941.4.2.167
CrossRef Full Text | Google Scholar
Ruscheweyh, R., Ikeda, H., Heinke, B., and Sandkuhler, J. (2004). Distinctive membrane and discharge properties of rat spinal lamina I projection neurones in vitro. J. Physiol. 555, 527–543. doi: 10.1113/jphysiol.2003.054049
PubMed Abstract | CrossRef Full Text | Google Scholar
Shepherd, G. M. (2004). The synaptic organization of the brain. New York: Oxford Univeristy Press.
Google Scholar
Smith, K. M., Browne, T. J., Davis, O. C., Coyle, A., Boyle, K. A., Watanabe, M., et al. (2019). Calretinin positive neurons form an excitatory amplifier network in the spinal cord dorsal horn. eLife 8:e49190. doi: 10.7554/eLife.49190
PubMed Abstract | CrossRef Full Text | Google Scholar
Spike, R. C., Puskar, Z., Andrew, D., and Todd, A. J. (2003). A quantitative and morphological study of projection neurons in lamina I of the rat lumbar spinal cord. Eur. J. Neurosci. 18, 2433–2448. doi: 10.1046/j.1460-9568.2003.02981.x
PubMed Abstract | CrossRef Full Text | Google Scholar
Suzuki, R., Rahman, W., Hunt, S. P., and Dickenson, A. H. (2004). Descending facilitatory control of mechanically evoked responses is enhanced in deep dorsal horn neurones following peripheral nerve injury. Brain Res. 1019, 68–76. doi: 10.1016/j.brainres.2004.05.108
PubMed Abstract | CrossRef Full Text | Google Scholar
Szucs, P., Luz, L. L., Lima, D., and Safronov, B. V. (2010). Local axon collaterals of lamina I projection neurons in the spinal cord of young rats. J. Comp. Neurol. 518, 2645–2665. doi: 10.1002/cne.22391
PubMed Abstract | CrossRef Full Text | Google Scholar
Szucs, P., Luz, L. L., Pinho, R., Aguiar, P., Antal, Z., Tiong, S. Y., et al. (2013). Axon diversity of lamina I local-circuit neurons in the lumbar spinal cord. J. Comp. Neurol. 521, 2719–2741. doi: 10.1002/cne.23311
PubMed Abstract | CrossRef Full Text | Google Scholar
Takazawa, T., and MacDermott, A. B. (2010). Synaptic pathways and inhibitory gates in the spinal cord dorsal horn. Ann. N. Y. Acad. Sci. 1198, 153–158. doi: 10.1111/j.1749-6632.2010.05501.x
PubMed Abstract | CrossRef Full Text | Google Scholar
Todd, A. J. (2017). Identifying functional populations among the interneurons in laminae I-III of the spinal dorsal horn. Mol. Pain 13:1744806917693003. doi: 10.1177/1744806917693003
PubMed Abstract | CrossRef Full Text | Google Scholar
Watt, A. J., Cuntz, H., Mori, M., Nusser, Z., Sjostrom, P. J., and Hausser, M. (2009). Traveling waves in developing cerebellar cortex mediated by asymmetrical Purkinje cell connectivity. Nat. Neurosci. 12, 463–473. doi: 10.1038/nn.2285
PubMed Abstract | CrossRef Full Text | Google Scholar
Weissman, T. A., and Pan, Y. A. (2015). Brainbow: new resources and emerging biological applications for multicolor genetic labeling and analysis. Genetics 199, 293–306. doi: 10.1534/genetics.114.172510
PubMed Abstract | CrossRef Full Text | Google Scholar
Wercberger, R., and Basbaum, A. I. (2019). Spinal cord projection neurons: a superficial, and also deep analysis. Curr. Opin. Physiol. 11, 109–115. doi: 10.1016/j.cophys.2019.10.002
PubMed Abstract | CrossRef Full Text | Google Scholar
Willis, W. D., Al-Chaer, E. D., Quast, M. J., and Westlund, K. N. (1999). A visceral pain pathway in the dorsal column of the spinal cord. Proc. Natl. Acad. Sci. U. S. A. 96, 7675–7679. doi: 10.1073/pnas.96.14.7675
PubMed Abstract | CrossRef Full Text | Google Scholar
Witter, L., Rudolph, S., Pressler, R. T., Lahlaf, S. I., and Regehr, W. G. (2016). Purkinje cell collaterals enable output signals from the cerebellar cortex to feed back to purkinje cells and interneurons. Neuron 91, 312–319. doi: 10.1016/j.neuron.2016.05.037
PubMed Abstract | CrossRef Full Text | Google Scholar
Yaksh, T. L. (1999). Regulation of spinal nociceptive processing: where we went when we wandered onto the path marked by the gate. Pain 6, S149–S152. doi: 10.1016/s0304-3959(99)00149-9
PubMed Abstract | CrossRef Full Text | Google Scholar
Yu, L. M., Polygalov, D., Wintzer, M. E., Chiang, M. C., and McHugh, T. J. (2016). CA3 synaptic silencing attenuates kainic acid-induced seizures and hippocampal network oscillations. eNeuro 3, ENEURO.0003–ENEURO.0016.2016. doi: 10.1523/ENEURO.0003-16.2016
PubMed Abstract | CrossRef Full Text | Google Scholar
Zeilhofer, H. U., Wildner, H., and Yevenes, G. E. (2012). Fast synaptic inhibition in spinal sensory processing and pain control. Physiol. Rev. 92, 193–235. doi: 10.1152/physrev.00043.2010
PubMed Abstract | CrossRef Full Text | Google Scholar
Zhang, C. K., Li, Z. H., Qiao, Y., Zhang, T., Lu, Y. C., Chen, T., et al. (2018). VGLUT1 or VGLUT2 mRNA-positive neurons in spinal trigeminal nucleus provide collateral projections to both the thalamus and the parabrachial nucleus in rats. Mol. Brain 11:22. doi: 10.1186/s13041-018-0362-y
PubMed Abstract | CrossRef Full Text | Google Scholar
Рассмотрим более подробно строение
отростков нейрона и различия между
ними. Как уже было сказано, определяющее
отличие отростков — функциональное,
т.е. направление проведения нервного
импульса: по аксону он проводится от
тела клетки, по дендриту — к телу.
Существует и ряд анатомических различий,
однако они не абсолютны и возможен ряд
исключений из них. Тем не менее, для
типичных аксонов и дендритов характерны
следующие признаки:
-
Аксон один, а дендритов несколько (хотя
существуют нейроны и с одним дендритом). -
Дендрит короче аксона. Длина дендрита
обычно не более700 мкм, а аксон может
достигать длины 1 м. -
Дендрит плавно отходит от
тела нейрона и постепенно истончается.
Аксон, отходя от тела клетки, практически
не меняет диаметр на всем своем
протяжении. Диаметр различных аксонов
колеблется от 0,3 до 16 мкм. От их толщины
зависит скорость проведения нервного
импульса — чем аксон толще, тем скорость
больше. Участок, примыкающий к телу
нейрона (аксонный холмик), имеет большую
толщину, чем остальная часть аксона. -
Дендриты ветвятся на всем
своем протяжении под острым углом,
дихотомически (вильчато), ветвление
начинается от тела клетки. Аксон обычно
ветвится только на конце, образуя
контакты (синапсы) с другими клетками.
Конечные разветвления аксона называют
терминалами. В некоторых местах от
аксонов могут отходить под прямым углом
тонкие ответвления — коллатерали. -
Дендриты (по крайней мере,
в ЦНС) не имеют миелиновой оболочки,
аксоны часто окружены миелиновой
оболочкой (о миелиновой оболочке см.
ниже).
Кроме того, иногда на веточках
дендрита есть выросты
— шипики, являющиеся
характерной структурной особенностью
дендритов, особенно в коре больших
полушарий (рис. 6). Шипик состоит из двух
частей — тела и головки, размеры и форма
которых варьируют. Шипики значительно
увеличивают постсинаптическую поверхность
дендрита. Они являются лабильными
образованиями и при различных воздействиях
(или разных функциональных состояниях)
могут менять свою конфигурацию,
дегенерировать и вновь появляться. В
результате увеличивается либо уменьшается
число синапсов, меняется эффективность
передачи в них нервного сигнала и т.д.
Рис. 6. Шипик на
дендрите нейрона и контактирующие с
ним пресинаптические окончания. Стрелками
показано направление проведения
информации
Теперь, когда мы рассмотрели
строение дендритов и аксонов, следует
несколько детальнее изучить строение
синапса. Синапс, состоящий из одного
пре- и одного постсинаптического
окончаний, называют простым. Однако
большинство синапсов в ЦНС являются
сложными. В таких синапсах один аксон
может контактировать сразу с несколькими
дендритами благодаря нескольким
мембранным выростам на его окончании.
И наоборот, один дендрит за счет своих
шипиков может контактировать с несколькими
аксонами. Еще более сложную структуру
имеют синаптические гломерулы
(клубочки)— компактные
скопления окончаний нервных отростков
разных клеток, формирующие большое
количество взаимных синапсов. Обычно
гломерулы окружены оболочкой из глиальных
клеток. Особенно характерно присутствие
гломерул в тех зонах мозга, где происходит
наиболее сложная обработка сигналов —
в коре больших полушарий и мозжечка, в
таламусе.
Итак, нейрон состоит из тела
(сомы) и отростков. Как правило, один из
отростков существенно длиннее остальных.
Такой длинный отросток называют нервным
волокном. В ЦНС это
всегда аксон; в периферической нервной
системе это может быть как аксон, так и
дендрит. По волокнам проводятся нервные
импульсы, имеющие электрическую природу,
в связи с чем, каждое волокно нуждается
в изолирующей оболочке.
По типу такой оболочки все
волокна делятся на миелиновые
(мякотные) и безмиелиновые
(безмякотные).
Безмиелиновые нервные волокна покрыты
только оболочкой, образованной телом
шванновской (нейроглиальной) клетки.
Эти волокна имеют малый диаметр и
полностью либо частично погружены во
впячивание шванновской клетки. Одна
шванновская клетка может образовывать
оболочку вокруг нескольких аксонов
разного диаметра. Такие волокна называются
волокнами кабельного типа (рис. 7). Так
как длина аксона существенно больше
размеров шванновских клеток, оболочку
аксона образуют цепочки нейроглиальных
клеток. Скорость проведения нервного
импульса по таким волокнам — 0,5-2 м/с.
Многие нервные волокна
имеют миелиновую оболочку. Она также
образуется нейроглиальными клетками.
При формировании такой оболочки
олигодендроцит (в ЦНС) или шванновская
клетка (в периферической нервной системе)
обхватывает участок нервного волокна
(рис. 8). После этого образуется вырост
в виде язычка, который закручивается
вокруг волокна, образуя мембранные слои
(цитоплазма при этом из «язычка»
выдавливается). Таким образом, миелиновая
оболочка представляет собой двойные
слои клеточной мембраны и по своему
химическому составу является липопротеидом,
т.е. соединением липидов (жироподобных
веществ) и белков. Миелиновая оболочка
осуществляет электрическую
изоляцию нервного волокна наиболее
эффективно. Нервный импульс проводится
по такому волокну быстрее,
чем по лишенному миелина (скорость
проведения может достигать
120 м/с). Миелиновая оболочка начинается
немного
отступя от тела нейрона и заканчивается
примерно в 2
мкм от синапса. Она состоит из цилиндров
длиной 1,5-2
мм,
каждый из которых образован своей
глиальной клеткой.
Цилиндры разделяют перехваты Ранвье —
не покрытые
миелином участки волокна (их длина 0,5 —
2,5 мкм), играющие большую роль в быстром
проведении нервного импульса. В перехватах
от аксона могут отходить коллатерали.
Поверх миелиновой оболочки у мякотных
волокон есть еще
наружная оболочка — неврилемма,
образованная цитоплазмой и ядром
нейроглиальных клеток.
Рис. 7. Строение
нервных волокон:
А
—
миелиновое;
Б
—
безмиелиновая;
I
—
волокно;
2 —
миелиновый
слой; 3—
ядро
шванновской клетки; 4 —
микротрубочки;
5—Нейрофиламенты;
6 —
митохондрии;
7—соединительнотканная
оболочка
Рис.
8.
Строение миелиновой оболочки (А).
Образование
миелиновой оболочки шванновской клеткой
(Б): ‘
1
—
аксон;
2 —
слои
миелиновой оболочки; 3
— перехваты
Ранвье;
4
—
ядро
шванновской клетки. Стрелкой показано
направление
продвижения
выроста цитоплазматической мембраны
Миелин
имеет белый цвет. Именно это его свойство
позволило
разделить вещество нервной системы на
серое и белое. Тела
нейронов и их короткие отростки образуют
более темное серое
вещество, а
волокна — белое
вещество.
-
Классификация
нейронов
Нейроны очень
разнообразны по форме, величине,
количеству и способу отхождения от тела
отростков, химическому строению (имеется
в виду, в первую очередь, синтез тех или
иных нейромедиаторов) и т.д. (рис. 9). Тела
самых крупных нейронов достигают в
диаметре 100 — 120 мкм (гигантские пирамиды
Беца в коре больших полушарий), самых
мелких — 4-5 мкм (зернистые клетки коры
мозжечка). Приведем основные способы
классификации нервных клеток.
Рис.
9.
Различные типы нейронов:
А
—
псевдоуниполярный
нейрон спинномозгового ганглия;
Б
—
биполярный
нейрон сетчатки; В —
мотонейрон
спинного мозга;
Г
—
пирамидная
клетка коры больших полушарий (видно,
что дендриты покрыты
шипиками); Д —
клетка
Пуркинье мозжечка; I
—
тело
клетки;
2
—
дендрит;
3 —
аксон;
4 —
коллатерали
аксона
-
Функционально
нейроны подразделяются на чувствительные
(сенсорные), вставочные (переключательные,
интернейроны)
и исполнительные (двигательные или
мотонейроны и
др.). Сенсорные
нейроны —
это нервные клетки, воспринимающие
раздражения из внешней или внутренней
среды организма.
Интернейроны
(вставочные
нейроны) обеспечивают связь
между чувствительными и исполнительными
нейронами рефлекторных дугах. Общее
направление эволюции нервной системы
связано с увеличением числа интернейронов.
Из более
чем ста миллиардов нейронов человека
более 70% составляют
вставочные нейроны.
Исполнительные
нейроны,
управляющие сокращениями поперечно —
полосатых мышечных волокон, называют
двигательными
(мотонейронами). Они
образуют нервно-мышечные синапсы.
Исполнительные нейроны, называемые
вегетативными, управляют
работой внутренних органов, включая
гладкомышечные волокна, железистые
клетки и др.
2. По количеству отростков
нейроны делятся на униполярные,
псевдоуниполярные, биполярные и
мультиполярные.Большинство
нейронов нервной системы (и почти все
нейроны в ЦНС) — это мультиполярные
нейроны (см.
рис. 9, В — Д), они имеют
один аксон и несколько дендритов.
Биполярные
нейроны (см.
рис. 9, Б) имеют один аксон и один дендрит
и характерны для
периферических отделов анализаторных
систем. Униполярных
нейронов, имеющих только один отросток,
у человека практически
нет. Из тела псевдоуниполярного
нейрона (см.
рис.9,
А) выходит один отросток, который
практически сразу делится
на две ветви. Одна из них выполняет
функцию дендрита, а
другая — аксона. Такие нейроны находятся
в чувствительных спинномозговых
и черепных ганглиях. Их дендрит
морфологически
(по строению) похож на аксон: он гораздо
длиннее аксона и часто имеет миелиновую
оболочку.
3. По форме тела и характеру
ветвления отростков выделяют звездчатые,
пирамидные, веретеновидные, корзинчатые,
зернистые
и др. нейроны.
-
По длине аксона нейроны делят
на клетки типа Гольджи I и типа Гольджи
II (эта классификация разработана
итальянским ученым К.
Гольджи). Клетки Гольджи I
имеют длинный
аксон, выходящий за пределы области, в
которой находится
тело нейрона. Это, например, пирамидные
клетки коры
больших полушарий. У клеток Гольджи II
короткий и, как
правило, очень разветвленный аксон, не
выходящий за пределы
области, в которой находится тело
нейрона. Примером
таких нейронов могут быть корзинчатые
клетки коры мозжечка. -
Каждый нейрон синтезирует
только один основной нейромедиатор.
Для того чтобы определить нервную
клетку с этой
точки зрения к названию медиатора
добавляют окончание
«-ергический». Например, ацетилхолинергический
нейрон образует ацетилхолин,
глицинергический — глицин и т.д.
Соседние файлы в предмете Анатомия и физиология
- #
01.06.201515.58 Mб544ОТ НЕЙРОНА К МОЗГУ.doc
- #
- #
- #
- #
- #
Текущая страница: 10 (всего у книги 20 страниц) [доступный отрывок для чтения: 5 страниц]
· аксосоматические синапсы;
· сомасоматические синапсы;
· дендродендритические синапсы;
III. По составу медиатора:
· адренергические синапсы – норадреналин;
· холинергические синапсы – ацетилхолин;
· пептидергические синапсы;
· пуринергические синапсы;
· дофаминергические синапсы;
IV. По выполняемым функциям:
· возбуждающие;
· тормозящие.
ЛЕКЦИЯ 12. Органы нервной системы
1. Структура нервной системы
2. Рефлекторная дуга
3. Нервы
4. Спинной мозг
5. Ствол мозга
6. Мозжечок
7. Кора больших полушарий головного мозга
8. Миелоархитектоника и организация коры
9. Строение и функции желудочков мозга
10. Мозговые оболочки
1. Нервная система осуществляет объединение частей организма в единое целое (интеграцию), обеспечивает регуляцию разнообразных процессов, координацию функции различных органов и тканей и взаимодействие организма с внешней средой. Нервная система воспринимает многообразную информацию, поступающую из внешней среды и из внутренних органов, перерабатывает ее и генерирует сигналы, обеспечивающие ответные реакции, адекватные действующим раздражителям.
Анатомически нервную систему подразделяют на:
· центральную нервную систему, которая включает в себя головной и спинной мозг;
· периферическую нервную систему, к которой относят периферические нервные узлы (ганглии), нервы и нервные окончания.
Физиологически (в зависимости от характера иннервации органов и тканей) нервную систему разделяют на:
· соматическую (анимальную) нервную систему, которая регулирует преимущественно функции произвольного движения;
· автономную (вегетативную) нервную систему, которая регулирует деятельность внутренних органов и желез. Влияя на активность обмена веществ в различных органах и тканях в соответствии с меняющимися условиями их функционирования и внешней среды, она осуществляет адаптационно-трофическую функцию.
Вегетативная нервная система подразделяется на взаимодействующие друг с другом симпатический и парасимпатический отделы, которые различаются локализацией центров в мозге и периферических узлов, а также характером влияния на внутренние органы.
В соматическую и автономную нервную систему входят звенья, расположенные в центральной и периферической нервных системах.
Функционально ведущей тканью органов нервной системы является нервная ткань, включающая нейроны и глию. Скопление нейронов в центральной нервной системе обычно называются ядрами, а в периферической нервной системе – узлами (ганглиями). Пучки нервных волокон в центральной нервной системе носят название трактов, в периферической нервной системе они образуют нервы.
Нервные центры – скопление нервных клеток в центральной и периферической нервных системах, в которых между ними осуществляется синаптическая передача. Они обладают сложной структурой, богатством и разнообразием внутренних и внешних связей и специализированы на выполнении определенных функций.
По характеру морфофункциональной организации различают:
· нервные центры ядерного типа, в которых нейроны располагаются без видимой упорядоченности (вегетативные ганглии, ядра спинного и головного мозга);
· нервные центры экранного типа, в которых нейроны, выполняющие однотипные функции, собраны в виде отдельных слоев, сходных с экранами, на которых проецируются нервные импульсы (кора мозжечка, кора полушарий большого мозга, сетчатка глаза). Внутри слоев и между ними имеются многочисленные ассоциативные связи.
В нервных центрах происходят процессы конвергенции и дивергенции нервного возбуждения, функционируют механизмы обратной связи.
Конвергенция – схождение различных путей проведения нервных импульсов к меньшему числу нервных клеток. На нейронах могут иметься окончания клеток разных типов, что обеспечивает конвергенцию влияний из различных источников.
Дивергенция – образование связей одного нейрона с большим числом других, на деятельность которых он оказывает влияние, обеспечивая перераспределение импульсов с иррадиацией возбуждения.
Механизмы обратной связи дают возможность нейронам самим регулировать величину поступающих к ним сигналов благодаря связям их аксонных коллатералей со вставочными клетками. Последние оказывают влияние (обычно тормозное) как на нейроны, так и на терминали конвергирующих к ним волокон.
2. Рефлекторная дуга является функциональной единицей нервной системы, они представляют собой цепочки нейронов, которые обеспечивают реакции рабочих органов (органов-мишеней) в ответ на раздражение рецепторов. В рефлекторных дугах нейроны, связанные друг с другом синапсами, образуют три звена: рецепторное (афферентное), эффекторное и расположенное между ними ассоциативное (вставочное), которое в простейшем варианте дуги может отсутствовать. На различные звенья дуги оказывают регуляторные воздействия связанные с ними нейроны вышележащих центров, вследствие чего рефлекторные дуги имеют сложное строение. Рефлекторные дуги в соматическом (анимальном) и автономном (вегетативном) отделах нервной системы обладают рядом особенностей.
Соматическая (анимальная) рефлекторная дуга
Рецепторное звено образовано афферентными псевдоуниполярными нейронами, тела которых располагаются в спинальных ганглиях. Дендриты этих клеток образуют чувствительные нервные окончания в коже или скелетной мускулатуре, а аксоны вступают в спинной мозг в составе задних корешков и направляются в задние рога его серого вещества, образуя синапсы на телах и дендритах вставочных нейронов. Некоторые веточки (коллатерали) аксонов псевдоуниполярных нейронов проходят (не образуя связей в задних рогах) непосредственно в передние рога, где оканчиваются на мотонейронах (формируя с ними двухнейронные рефлекторные дуги).
Ассоциативное звено представлено мультиполярными вставочными нейронами, дендриты и тела которых расположены в задних рогах спинного мозга, а аксоны направляются в передние рога, передавая импульсы на тела и дендриты эффекторных нейронов.
Эффекторное звено образовано мультиполярными мотонейронами, тела и дендриты которых лежат в передних рогах, а аксоны выходят из спинного мозга в составе передних корешков, направляются к спинальному ганглию и далее в составе смешанного нерва – к скелетной мышце, на волокнах которой их веточки образуют нервно-мышечные синапсы (моторные, или двигательные, бляшки).
Автономная (вегетативная) рефлекторная дуга
Рецепторное звено, как и в соматической рефлекторной дуге, образовано афферентными псевдоуниполярными нейронами, тела которых располагаются в спинальных ганглиях, однако дендриты этих клеток образуют чувствительные нервные окончания в тканях внутренних органов, сосудов и желез. Их аксоны вступают в спинной мозг в составе задних корешков и, минуя задние рога, направляются в боковые рога серого вещества, образуя синапсы на телах и дендритах вставочных нейронов.
Ассоциативное звено представлено мультиполярными вставочными нейронами, дендриты и тела которых расположены в боковых рогах спинного мозга, а аксоны (преганглинарные волокна) покидают спинной мозг в составе передних корешков, направляясь в один из вегетативных ганглиев, где и оканчивается на дендритах и телах эффекторных нейронов.
Эффекторное звено образовано мультиполярными нейронами, тела которых лежат в составе вегетативных ганглиев, а аксоны (постганглионарные волокна) в составе нервных стволов и их ветвей направляются к клеткам рабочих органов – гладких мышц, желез, сердца.
3. Нервы
Нервы (нервные стволы) связывают нервные центры головного и спинного мозга с рецепторами и рабочими органами. Они образованы пучками нервных волокон, которые объединены соединительнотканными компонентами (оболочками): эндоневрием, периневрием и эпиневрием. Большинство нервов являются смешанными, то есть включают афферентные и эфферентные нервные волокна. Пучки нервных волокон содержат до нескольких тысяч миелиновых и безмиелиновых волокон, соотношение между которыми в различных нервах неодинаково; по функциональному признаку они относятся к анимальной и вегетативной нервной системе.
Эндоневрий – тонкие прослойки рыхлой волокнистой соединительной ткани, окружающие отдельные нервные волокна и связывающие их в единый пучок. В нем содержатся немногочисленные клетки и волокна (преимущественно ретикулярные), проходят мелкие кровеносные сосуды.
Периневрий – оболочка, покрывающая каждый пучок нервных волокон снаружи и отдающая перегородки вглубь пучка. Он образован 2-10 концентрическими пластами уплощенных клеток, связанных плотными и щелевыми соединениями. Цитоплазма клеток, в особенности наружных слоев, содержит многочисленные пиноцитозные пузырьки. Между слоями клеток в щелевидных пространствах, заполненных жидкостью, располагаются компоненты базальной мембраны и продольно ориентированные коллагеновые волокна. В терминальной части нерва периневрий образован лишь одним слоем плоских клеток, который дистально резко обрывается и имеет вид открытой манжетки.
Эпиневрий – это наружная оболочка нерва, связывающая воедино пучки нервных волокон (число которых зависит от диаметра нерва и варьирует от одного до нескольких десятков). Он состоит из плотной волокнистой соединительной ткани, содержащей жировые клетки, кровеносные и лимфатические сосуды.
Нервные узлы
Нервные узлы (ганглии) – скопление нейронов вне центральной нервной системы. Они разделяются на чувствительные (сенсорные) и автономные (вегетативные).
Чувствительные (сенсорные)нервные узлы содержат псевдоуниполярные или биполярные (в спиральном и вестибулярном ганглиях) афферентные нейроны и располагаются по ходу задних корешков спинного мозга (спинномозговые, или спинальные, узлы) и черепномозговых нервов (5, 7, 8, 9, 10).
Спинномозговые узлы
Спинномозговой (спинальный) узел (ганглий) имеет веретеновидную форму и покрыт капсулой из плотной волокнистой соединительной ткани. По его периферии находятся плотные скопления тел псевдоуниполярных нейронов, а центральная часть занята их отростками и расположенными между ними тонкими прослойками эндоневрия, несущими сосуды.
Псевдоуниполярные нейроны характеризуются сферическим телом и светлым ядром с хорошо заметным ядрышком. Выделяют крупные и мелкие клетки, которые, вероятно, различаются видами проводимых импульсов. Цитоплазма нейронов содержит многочисленные митохондрии, цистерны гранулярной эндоплазматической сети, элементы комплекса Гольджи, лизосомы. Каждый нейрон окружен слоем прилежащих к нему уплощенных клеток олигодендроглии (мантийными глиоцитами, или клетками-сателлитами) с мелкими округлыми ядрами; снаружи от глиальной оболочки имеется тонкая соединительнотканная оболочка. От тела псевдоуниполярного нейрона отходит отросток, разделяющийся Т-образно на афферентную (дендритную) и эфферентную (аксональную) ветви, которые покрываются миелиновыми оболочками. Афферентная ветвь заканчивается на периферии рецепторами, эфферентная в составе заднего корешка вступает в спинной мозг. Так как переключения нервного импульса с одного нейрона на другой в пределах спинномозговых узлов не происходит, они не являются нервными центрами. Нейроны спинномозговых узлов содержат такие нейромедиаторы как ацетилхолин, глутаминовая кислота, вещество Р, соматостатин, холецистокинин, гастрин, вазоинтестинальный пептид.
Автономные (вегетативные) узлы
Автономные (вегетативные) нервные узлы (ганглии) могут располагаться вдоль позвоночника (паравертебральные ганглии), или впереди него (превертебральные ганглии), а также в стенке органов – сердца, бронхов, пищеварительного тракта, мочевого пузыря и других (интрамуральные ганглии) или вблизи их поверхности. Иногда они имеют вид мелких (от нескольких клеток до нескольких десятков клеток) скоплений нейронов, расположенных по ходу некоторых нервов или лежащих интрамурально (микроганглии). К вегетативным узлам подходят преганглионарные волокна (миелиновые), содержащие отростки клеток, тела которых лежат в центральной нервной системе. Эти волокна сильно ветвятся и образуют многочисленные синаптические окончания на клетках вегетативных узлов. Благодаря этому осуществляется конвергенция большого числа терминалей преганглионарных волокон на каждый нейрон ганглия. В связи с наличием синаптической передачи вегетативные узлы относят к нервным центрам ядерного типа.
Вегетативные нервные узлы по функциональному признаку и локализации разделяются на симпатические и парасимпатические.
Симпатические нервные узлы (пара– и превертебральные) получают преганглионарные волокна от клеток, расположенных в вегетативных ядрах грудных и поясничных сегментов спинного мозга. Нейромедиатором преганглионарных волокон является ацетилхолин, а постганглионарных – норадреналин (за исключением потовых желез и некоторых кровеносных сосудов, имеющих холинергическую симпатическую иннервацию). Помимо этих нейромедиаторов, в узлах выявляются энкефалины, вещество Р, соматостатин, холецистокинин.
Парасимпатические нервные узлы (интрамуральные, лежащие вблизи органов или узлы головы) получают преганглионарные волокна от клеток, расположенных в вегетативных ядрах продолговатого и среднего мозга, а также крестцового отдела спинного мозга. Эти волокна покидают центральную нервную систему в составе 3, 7, 9, 10 пар черепномозговых нервов и передних корешков крестцовых сегментов спинного мозга. Нейромедиатором пре– и постганглионарных волокон является ацетилхолин. Кроме него роль медиаторов в этих ганглиях играют серотонин, АТФ, возможно, некоторые пептиды.
Большинство внутренних органов имеет двойную вегетативную иннервацию, то есть получают постганглионарные волокна от клеток, расположенных как в симпатических, так и в парасимпатических узлах. Реакции, опосредуемые клетками симпатических и парасимпатических узлов, часто имеют противоположную направленность, например: симпатическая стимуляция усиливает, а парасимпатическая – тормозит сердечную деятельность.
Общий план строения симпатических и парасимпатических нервных узлов сходен. Вегетативный узел покрыт соединительнотканной капсулой и содержит диффузно или группами расположенные тела мультиполярных нейронов, их отростки в виде безмиелиновых или, реже, миелиновых волокон и эндоневрий. Тела нейронов имеют неправильную форму, содержат эксцентрично расположенное ядро, окружены (обычно не полностью) оболочками из глиальных клеток-сателлитов (мантийных глиоцитов). Часто встречаются многоядерные и полиплоидные нейроны.
Интрамуральные узлы и связанные с ними проводящие пути в виду их высокой автономии, сложности организации и особенностей медиаторного обмена некоторыми авторами выделяются в самостоятельный метасимпатический отдел вегетативной нервной системы. В частности, общее число нейронов в интрамуральных узлах кишки выше, чем в спинном мозге, а по сложности их взаимодействия в регуляции перистальтики и секреции их сравнивают с миникомпьютером.
В интрамуральных узлах описаны нейроны трех типов:
· длинноаксонные эфферентные нейроны (клетки Догеля I типа) численно преобладают. Это крупные или средних размеров эфферентные нейроны с короткими дендритами и длинным аксоном, направляющимся за пределы к рабочему органу, на клетках которого он образует двигательные или секреторные окончания;
· равноотростчатые афферентные нейроны (клетки Догеля II типа) содержат длинные дендриты и аксон, уходящий за пределы данного ганглия в соседние и образующий синапсы на клетках I и III типов. Эти клетки, по-видимому, входят в качестве рецепторного звена в состав местных рефлекторных дуг, которые замыкаются без захода нервного импульса в центральную нервную систему. Наличие таких дуг подтверждается сохранением функционально активных афферентных, ассоциативных и эфферентных нейронов в трансплантированных органах (например, сердце);
· ассоциативные клетки (клетки Догеля III типа) – местные вставочные нейроны, соединяющие своими отростками несколько клеток I и II типа, морфологически сходные с клетками Догеля II типа. Дендриты этих клеток не выходят за пределы узла, а аксоны направляются в другие узлы, образуя синапсы на клетках I типа.
4. Спинной мозг располагается в позвоночном канале и имеет вид округлого тяжа, расширенного в шейном и поясничном отделах и пронизанного центральным каналом. Он состоит из двух симметричных половин, разделенных спереди срединной щелью, сзади срединной бороздой, и характеризуется сегментарным строением; с каждым сегментом связана пара передних (вентральных) и пара задних (дорсальных) корешков. В спинном мозге различают серое вещество, расположенное в его центральной части, и белое вещество, лежащее по периферии.
Серое вещество на поперечном разрезе имеет вид бабочки и включает парные передние (вентральные), задние (дорсальные) и боковые (латеральные) рога (в действительности представляют собой непрерывные столбы, идущие вдоль спинного мозга). Рога серого вещества обеих симметричных частей спинного мозга связаны друг с другом в области центральной серой комиссуры (спайки). В сером веществе находятся тела, дендриты и (частично) аксоны нейронов, а также глиальные клетки. Между телами нейронов находится нейропиль – сеть, образованная нервными волокнами и отростками глиальных клеток.
Цитоархитектоника спинного мозга
Нейроны располагаются в сером веществе в виде не всегда резко разграниченных скоплений (ядер), в которых происходит переключение нервных импульсов с клетки на клетку (отчего их относят к нервным центрам ядерного типа). В зависимости от топографии аксонов нейроны спинного мозга подразделяются на:
· корешковые нейроны, аксоны которых образуют передние корешки;
· внутренние нейроны, отростки которых заканчиваются в пределах серого вещества спинного мозга;
· пучковые нейроны, отростки которых образуют пучки волокон в белом веществе спинного мозга в составе проводящих путей.
Задние рога содержат несколько ядер, образованных мультиполярными вставочными нейронами мелких и средних размеров, на которых оканчиваются аксоны псевдоуниполярных клеток спинальных ганглиев, несущие разнообразную информацию от рецепторов, а также волокна нисходящих путей из лежащих выше (супраспинальных) центров. В задних рогах выявляются высокие концентрации таких нейромедиаторов, как серотонин, энкефалин, вещество Р.
Аксоны вставочных нейронов:
· оканчиваются в сером веществе спинного мозга на мотонейронах, лежащих в передних рогах;
· образуют межсегментарные связи в пределах серого вещества спинного мозга;
· выходят в белое вещество спинного мозга, где образуют восходящие и нисходящие проводящие пути, часть аксонов при этом переходит на противоположную сторону спинного мозга.
Боковые рога хорошо выражены на уровне грудных и крестцовых сегментов спинного мозга, содержат ядра, образованные телами вставочных нейронов, которые относятся к симпатическому и парасимпатическому отделам вегетативной нервной системы. На дендритах и телах этих клеток оканчиваются аксоны:
· псевдоуниполярных нейронов, несущих импульсы от рецепторов, расположенных во внутренних органах;
· нейронов центров регуляции вегетативных функций, тела которых находятся в продолговатом мозге.
Аксоны вегетативных нейронов, выходя из спинного мозга в составе передних корешков, образуют преганглионарные волокна, направляющиеся к симпатическим и парасимпатическим узлам. В нейронах боковых рогов основным медиатором является ацетилхолин, выявляется также ряд нейропептидов – энкефалин, нейротензин, вещество Р, соматостатин.
Передние рога содержат мультиполярные двигательные клетки (мотонейроны) общим числом около 2–3 млн. Мотонейроны объединяются в ядра, каждое их которых обычно тянется на несколько сегментов. Различают крупные (диаметр тела 35–70 мкм) альфа-мотонейроны и рассеянные среди них более мелкие (15–35 мкм) гамма-мотонейроны.
На отростках и телах мотонейронов имеются многочисленные синапсы (до нескольких десятков тысяч на каждом), оказывающие на них возбуждающие и тормозные воздействия. На мотонейронах оканчиваются:
· коллатерали аксонов псевдоуниполярных клеток спинальных узлов, образующие с ними двухнейронные (моносинаптические) рефлекторные дуги;
· аксоны вставочных нейронов, тела которых лежат в задних рогах спинного мозга;
· аксоны клеток Реншоу, образующие тормозные аксо-соматические синапсы. Тела этих мелких вставочных нейронов располагаются в середине переднего рога и иннервированы коллатералями аксонов мотонейронов;
· волокна нисходящих путей пирамидной и экстрапирамидной систем, несущие импульсы из коры большого мозга и ядер ствола мозга.
Гамма-мотонейроны, в отличие от альфа-мотонейронов, не имеют непосредственной связи с чувствительными нейронами спинальных узлов.
Аксоны альфа-мотонейронов отдают коллатерали, оканчивающиеся на телах вставочных клеток Реншоу, и покидают спинной мозг в составе передних корешков, направляясь в смешанных нервах к соматическим мышцам, на которых они заканчиваются нервномышечными синапсами (моторными бляшками). Более тонкие аксоны гамма-мотонейронов имеют такой же ход и образуют окончания на интрафузальных волокнах нервно-мышечных веретен. Нейромедиатором клеток передних рогов является ацетилхолин.
Центральный спинномозговой канал проходит в центре серого вещества в центральной серой комиссуре (спайке). Он заполнен спинномозговой жидкость и выстлан одним слоем кубических или призматических клеток эпендимы, апикальная поверхность которых покрыта микроворсинками и (частично) ресничками, а латеральные связаны комплексами межклеточных соединений.
Белое вещество спинного мозга окружает серое и разделяется передними и задними корешками на симметричные дорсальные, латеральные и вентральные канатики. Оно состоит из продольно идущих нервных волокон (преимущественно миелиновых), образующих нисходящие и восходящие проводящие пути (тракты). Последние отделены друг от друга тонкими прослойками соединительной ткани и астроцитов (встречаются и внутри трактов). Для каждого тракта характерно преобладание волокон, образованных однотипными нейронами, поэтому тракты существенно различаются содержащимися в их волокнах нейромедиаторами и (как и нейроны) подразделяются на моноаминергические, холинергические, глутаматергические, глицинергические и пептидергические. Проводящие пути включают две группы: проприоспинальные и супраспинальные пути.
Проприоспинальные проводящие пути собственные проводящие пути спинного мозга, которые образованы аксонами вставочных нейронов, они осуществляют связь между его различными отделами. Эти пути проходят, в основном, на границе белого и серого вещества в составе латеральных и вентральных канатиков.
Супраспинальные проводящие пути обеспечивают связь спинного мозга со структурами головного мозга и включают восходящие спинно-церебральные и нисходящие церебро-спинальные тракты.
Спинно-церебральные тракты обеспечивают передачу в головной мозг разнообразной сенсорной информации. Часть их этих 20 трактов образована аксонами клеток спинномозговых узлов, большинство же представлено аксонами различных вставочных нейронов, тела которых, расположены в той же или противоположной стороне спинного мозга.
Церебро-спинальные тракты обеспечивают связь головного мозга со спинным и включают пирамидную и экстрапирамидную системы.
Пирамидная система образована длинными аксонами пирамидных клеток коры большого мозга и насчитывает у человека около миллиона миелиновых волокон, которые на уровне продолговатого мозга большей частью переходят на противоположную сторону и формируют латеральный и вентральный кортико-спинальные тракты. Волокна этих трактов проецируются не только на мотонейроны, но и на вставочные нейроны серого вещества. Пирамидная система контролирует точные произвольные движения скелетной мускулатуры, в особенности конечностей.
Экстрапирамидная система образована нейронами, тела которых лежат в ядрах среднего и продолговатого мозга и моста, а аксоны оканчиваются на мотонейронах и вставочных нейронах. Она контролирует преимущественно тонус скелетных мышц, а также деятельность мышц, обеспечивающих поддержание позы и равновесия тела.
Наружная (поверхностная) пограничная глиальная мембрана, состоящая из слившихся уплощенных отросков астроцитов, образует внешнюю границу белого вещества спинного мозга, отделяющую центральную нервную систему от периферической нервной системы. Эту мембрану пронизывают нервные волокна, составляющие передние и задние корешки.
5. Ствол головного мозга
Головной мозг состоит из ствола мозга, который является продолжением спинного мозга (включает продолговатый, задний, средний и промежуточный мозг) и плащевой части, образованной полушариями большого мозга и мозжечком. В стволе головного мозга серое вещество представлено многочисленными ядрами, окруженными белым веществом: лишь в каудальном отделе продолговатого мозга еще обнаруживается продолжение передних и задних рогов спинного мозга, однако в краниальном направлении единые скопления нейронов разделяются проводящими путями, формируя ядра. От ствола отходят десять пар (с 3 по 12) черепно-мозговых нервов, ядра которых располагаются в пределах продолговатого и среднего мозга.
Ядра ствола мозга подразделяются на чувствительные, двигательные и ассоциативные.
Чувствительные ядра являются гомологами ядер задних рогов спинного мозга – в них сосредоточены тела и дендриты мультиполярных вставочных нейронов, на которых оканчиваются аксоны псевдоуниполярных или биполярных клеток, несущие сенсорную информацию.
Двигательные ядра содержат мотонейроны, аксоны которых оканчиваются на волокнах соматической мускулатуры. К двигательным ядрам часто относят и вегетативные ядра продолговатого и среднего мозга, содержащие тела нейронов, аксоны которых образуют преганглинарные волокна, направляющиеся в парасимпатические нервные узлы в составе 3, 7, 9, 10 пар черепно-мозговых нервов.
Ассоциативные (переключательные, релейные) ядра содержат скопления ассоциативных мультиполярных клеток, которые обеспечивают формирование многонейронных рефлекторных дуг путем переключения нервных импульсов, идущих к коре полушарий или мозжечка, или в обратном направленииот коры к стволу мозга и центрам спинного мозга.
Белое вещество ствола мозга имеет то же гистологическое строение, что и в спинном мозге и состоит из пучков нервных волокон, образующих восходящие и нисходящие тракты, которые связывают разные отделы центральной нервной системы. Наряду с особенностями топографии и строения, отдельные ядра ствола мозга и его проводящие пути различаются химической спецификой нейромедиаторов.
Особым отделом центральной нервной системы, обладающим специфической организацией и связывающим ее различные уровни, является ретикулярная формация.
Ретикулярная формация образована группами мелких, средних и крупных мультиполярных вставочных нейронов с различным характером ветвления дендритов и аксонов, содержащих различные нейромедиаторы и окруженных сетями нервных волокон. Она начинается в спинном мозге и протягивается до промежуточного, достигая в краниальном направлении все большего развития. При этом диффузное расположение ее элементов сменяется более компактным с формированием отдельных ядер, число которых, по разным классификациям, составляет от нескольких десятков до сотни.
Нейроны ретикулярной формации характеризуются большим количеством афферентных связей, идущих от сенсорных образований, и богатством эфферентных проекций. Их отростки направляются в кору больших полушарий, в ядра различных отделов ствола, конечного мозга и мозжечка, объединяя их в одну систему (интегративная функция ретикулярной формации).
Обширные восходящие проекции, в том числе, непосредственно в кору большого мозга, обеспечивают активирующее влияние ретикулярной формации на высшие центры нервной системы. Совокупность нисходящих проекций ретикулярной формации рассматривают как систему, угнетающую активность нижележащих центров. Основной объем этих проекций представлен волокнами ретикулоспинального тракта, которые угнетают активность мотонейронов спинного мозга. Ретикулярной формации приписывают участие в восприятии боли, агрессивном и половом поведении. Основными медиаторами в ней являются ацетилхолин, норадреналин, дофамин, серотонин.
Гипоталамус – участок промежуточного мозга, содержащий ядра, часть из которых объединяет тела особых нейронов, специализированных на выработке нейрогормонов. Последние транспортируются по аксонам и выделяются в капиллярную сеть срединного возвышения или нейрогипофиза. Таким образом, не все связи между центральной нервной системой и органами-мишенями осуществляются с помощью нервных волокон.
6. Мозжечок располагается над продолговатым мозгом и варолиевым мостом и представляет собой центр равновесия, поддержания мышечного тонуса, координации движений и контроля сложных и автоматически выполняемых двигательных актов. Он образован двумя полушариями с большим числом бороздок и извилин на поверхности и узкой средней частью (червем) и связан с другими частями мозга тремя парами ножек. Серое вещество образует кору мозжечка и ядра, которые залегают в глубине его белого вещества.
Кора мозжечка является нервным центром экранного типа и характеризуется высокой упорядоченностью расположения нейронов, нервных волокон и глиальных клеток. В ней различают три слоя (снаружи внутрь):
· молекулярный слой, содержащий сравнительно небольшое количество мелких клеток;
· ганглионарный слой, образованный одним рядом тел крупных грушевидных клеток (клеток Пуркинье);
· зернистый слой, с большим количеством плотно лежащих клеток.
Молекулярный слой содержит тела корзинчатых и звездчатых клеток (коротко– и длинноаксонных).
Корзинчатые клетки располагаются во внутренней части молекулярного слоя. Их короткие дендриты образуют связи с параллельными волокнами в наружной части молекулярного слоя, а длинный аксон идет поперек извилины, отдавая через определенные интервалы коллатерали, которые спускаются к телам клеток Пуркинье и, разветвляясь, охватывают их наподобие корзинок, образуя тормозные аксо-соматические синапсы.
Звездчатые клетки – мелкие нейроны, тела которых лежат выше тел корзинчатых клеток. У короткоаксонных звездчатых клеток дендриты образуют связи с параллельными волокнами, а разветвления аксона формируют тормозные синапсы на дендритах клеток Пуркинье. У длинноаксонных звездчатых клеток аксон может участвовать в образовании корзинки вокруг тела клетки Пуркинье.
Ганглионарный слой содержит лежащие в один ряд тела клеток Пуркинье (грушевидных нейронов), оплетенные коллатералями аксонов корзинчатых клеток («корзинками»).